题目内容
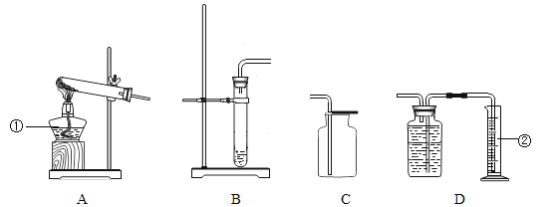
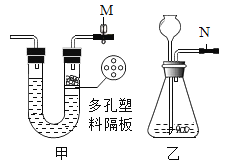
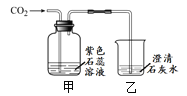
【题目】进行如图实验,研究物质的性质。

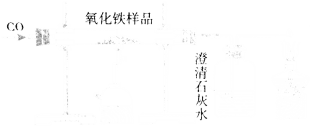
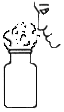
(1)A中的现象是______。
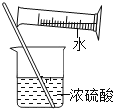
(2)B中反应的化学方程式为______。
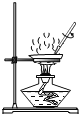
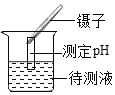
(3)C中滴入稀盐酸后得到溶液甲,向甲中继续滴加Ca(OH)2溶液,有白色沉淀生成。溶液甲中的溶质是______(填化学式)。
【答案】锌粒逐渐减少,有气泡产生 Fe2O3+6HCl===2FeCl3+3H2O Na2CO3、NaCl
【解析】
(1)锌和稀盐酸反应生成氯化锌和氢气,现象为锌粒逐渐减少,有气泡产生;
(2)氧化铁和稀盐酸反应生成氯化铁和水,反应的方程式为Fe2O3+6HCl===2FeCl3+3H2O;
(3)稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;向碳酸钠中滴入稀盐酸后得到溶液甲,向甲中继续滴加Ca(OH)2溶液,有白色沉淀生成,说明甲溶液中含有碳酸钠,说明稀盐酸为少量,所以甲中含有第一步反应剩余的碳酸钠,和第一步反应生成的氯化钠。

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
【题目】依据下列实验和数据回答下列问题。
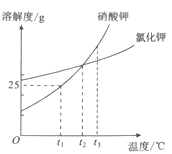
在下表对应的温度下,向4只盛有100 g水的烧杯中,分别加入40 g KCl固体,充分溶解。KCl的溶解度曲线如图。

烧杯序号 | ① | ② | ③ | ④ |
温度(℃) | 20 | 30 | 50 | 60 |
【1】①~④所得溶液属于饱和溶液的是()
A. ①② B. ②③ C. ③④ D. ①④
【2】下列关于①~④所得溶液的说法不正确的是()
A. 溶质质量 ①<② B. 溶液质量 ②<③
C. 溶质质量分数 ③<④ D. ④中溶质与溶剂的质量比为 2:5