题目内容
【题目】某课外活动小组对失去标签的稀硫酸浓度进行测定:取稀硫酸50 g于烧杯中,逐滴滴加3.42%的氢氧化钡溶液,烧杯内溶质质量与滴加氢氧化钡溶液质量关系如图所示。(结果保留两位小数)
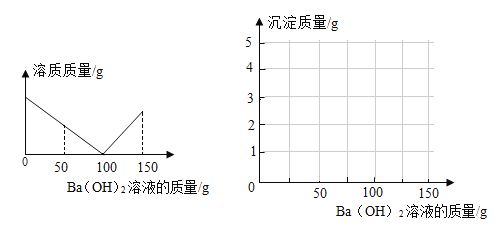
(1)参加反应的Ba(OH)2质量共有 g。当滴加Ba(OH)2溶液50g时,烧杯内溶液的pH 7(填“>”“<”或“=”)。
(2)求该硫酸溶液的溶质质量分数。
(3)通过计算,在图中画出产生沉淀质量与滴加Ba(OH)2溶液的质量关系。
(4)滴加Ba(OH)2溶液至150g时,所得溶液的溶质质量分数 。
【答案】(1)3.42; <;(2)3.92%(3)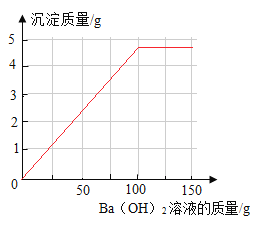 ;(4)0.88%
;(4)0.88%
【解析】
(1) 参加反应的Ba(OH)2质量共有![]() 。当滴加Ba(OH)2溶液50 g时,烧杯内还有硫酸剩余,所以溶液的pH<7;
。当滴加Ba(OH)2溶液50 g时,烧杯内还有硫酸剩余,所以溶液的pH<7;
(2)设稀硫酸的溶质质量分数为x。
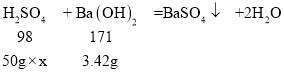
![]()
x=3.92%,稀硫酸的溶质质量分数为3.92%;
(3)设生成的BaSO4质量为y。
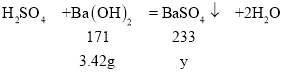
![]()
y=4.66g。
得到的沉淀关系图为:
(4) 滴加Ba(OH)2溶液至150g时,所得溶液的溶质质量分数=![]() ×100%≈0.88%。
×100%≈0.88%。

练习册系列答案
相关题目