题目内容
【题目】A、B、C三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中不正确的是( )

A.t1°C时,65gA 的饱和溶液中含有溶剂50g
B.t1°C时, 溶解度由大到小的顺序是: B>C>A
C.将t2°C时A、B、C三种物质的饱和溶液降温至t1°C时,C溶液中溶质的质量分数保持不变
D.t2°C时,A、B两种溶液中溶质的质量分数相同
【答案】D
【解析】
A、t1°C时,A的溶解度为30g,在100g的溶剂中能溶解30gA达饱和状态,故A正确;
B、根据溶解度曲线,t1°C时, 溶解度由大到小的顺序是: B>C>A,故B正确;
C、根据溶解度曲线,C的溶解度随温度升高而降低,那么降温过程C溶液中溶质的质量分数保持不变,故C正确;
D、t2°C时,A、B的溶解度相等,两种饱和溶液中溶质的质量分数相同,故D错误。
故选D

 阅读快车系列答案
阅读快车系列答案【题目】某学习小组在验证“氢氧化钙溶液导电性”的实验时,发现除了两根石墨电极表面分别产生氢气、氧气外,还出现了一个意外现象:容器内的澄清石灰水变浑浊。
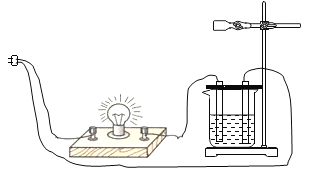
(提出问题)是什么原因导致澄清石灰水变浑浊?
(猜想与假设)他们分别对这种意外现象作如下猜想:
甲同学:________________。
乙同学:可能是电解过程中放热,温度升高使氢氧化钙固体析出;
丙同学:可能是石墨电极被通电时产生的活性氧氧化产生的CO2与石灰水反应产生了沉淀。
(设计实验)
(1)甲、乙、丙三位同学分别设计了如下实验。
实验步骤 | 实验现象 | 实验结论 |
甲:向装有10ml饱和澄清石灰水的烧杯中加入10ml蒸馏水,接通电源,计时3分钟 | a.两电极表面均产生气泡, 溶液体积几乎无变化; b. ___________________ | 甲同学猜想不正确 |
乙:__________________ | _______________________ | 乙同学猜想不正确 |
丙:将电解实验中产生的白色浑浊过滤,并向沉淀中加入足量的稀盐酸。 | _______________________ | 丙同学猜想正确 |
(2)产生白色浑浊的化学方程式为___________________________。
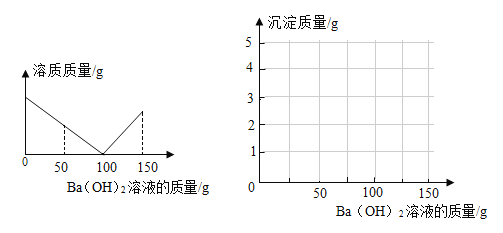
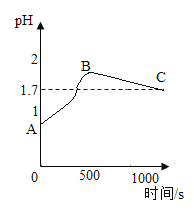
(3)丙同学实验后,为了防止废液中过量的盐酸污染环境,他按照传统方式向废液中加入过量的石灰石,并同时用pH传感器测整个过程的pH变化,即从开始反应到最终不再产生气体直至过量石灰石沉淀分层,静置一段时间后得到的图像如图所示。最终溶液pH为1.7,则C点时溶液中的溶质为______________(填化学式);AB段pH.上升的原因是________________;BC段变化的原因是_______;你对“在不同指示剂的情况下,用过量石灰石除去废液里的稀盐酸”这种方案的认识是___________________。
【题目】对比实验是实验探究的重要方法,下列对比实验设计能实现相应实验目的的是
选项 | 实验目的 | 实验设计 | 选项 | 实验目的 | 实验设计 |
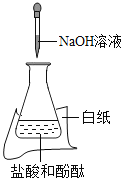
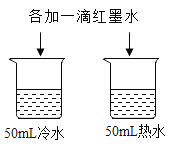
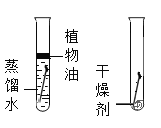
A | 探究温度对分子运动快慢的影响 |
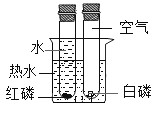
| B | 探究水对铁钉锈蚀的影响 |
|
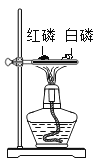
C | 探究空气是燃烧的必要条件 |
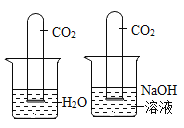
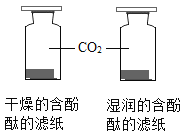
| D | 探究CO2与水反生反应 |
|
A. A B. B C. C D. D