题目内容
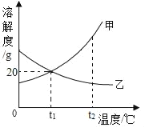
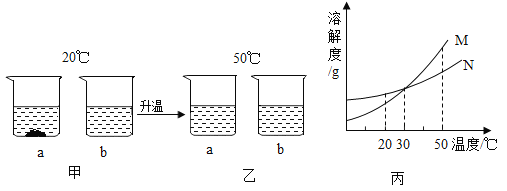
【题目】如图是甲、乙、丙三种固体物质的溶解度曲线,下列叙述正确的是
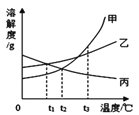
A. t2℃时,甲、丙两溶液中溶质的质量分数相等
B. 甲物质中混有少量乙物质,可用降温结晶的方法提纯甲
C. t3℃时,甲、乙、丙三种饱和溶液恒温蒸发等质量的水,则析出固体(不含水)的质量:甲>乙>丙
D. t3℃时,甲、乙两种饱和溶液降温到t2℃时析出固体的质量:甲>乙
【答案】BC
【解析】
A、没有确定溶液是否饱和,不能确定溶液中质量分数是否相等,t2℃时,甲、丙两饱和溶液中溶质的质量分数相等,故A错误;
B、甲的溶解度随温度的升高且增大明显,B的溶解度随温度的升高且增大不明显。甲中混有少量乙,可用降温结晶的方法提纯甲,故B正确;
C、t3℃时,甲、乙、丙的溶解度关系为甲>乙>丙,故甲、乙、丙三种饱和溶液恒温蒸发等质量的水,则析出固体(不含水)的质量:甲>乙>丙,故C正确;
D、没有确定溶液的质量,故t3℃甲乙两种饱和溶液降温到t2℃时析出固体的质量不能确定,故D错误。故选BC。

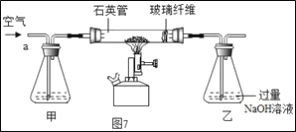
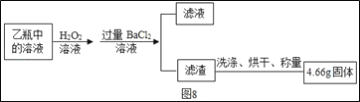
【题目】某化学兴趣小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后瓶中残留废液进行探究。
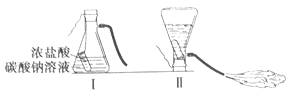
(提出问题)废液中所含溶质是什么?
(猜想与假设)
猜想1:废液中的溶质是NaCl、Na2CO3和HCl
猜想2:废液中的溶质只有NaCl
猜想3:废液中的溶质是NaCl、HCl
猜想4:废液中的溶质是______。
(讨论与交流)
小明认为猜想I无需验证就知道是错误的,他的理由是_____(请用化学方程式说明)。
(实验与结论)
(1)小亮同学为验证猜想3,取少量废液装入试管中,然后滴入酚酞溶液,发现溶液不变色,于是小亮认为猜想3正确。你认为他的结论____(填“正确”或“错误”),理由是______________。
请你另设计实验方案验证猜想3:
实验步骤 | 实验现象 | 实验结论 |
__________________ | __________________ | 猜想3正确 |
(2)验证猜想4,可选择的试剂有____________。
A.酚酞溶液B.氢氧化钾溶液C.稀硫酸D.氯化钡溶液
(拓展与应用)若废液中的溶质是NaCl和HCl,根据盐酸的性质,无需另加试剂,只要对废液进行____操作,即可从废液中得到NaCl固体。