��Ŀ����
����Ŀ��ij������Ʒ�к��������Ȼ�þ���Ȼ��ƣ�ijͬѧ����������ᴿ������
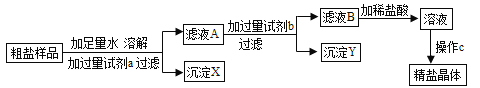
��ش��������⣺
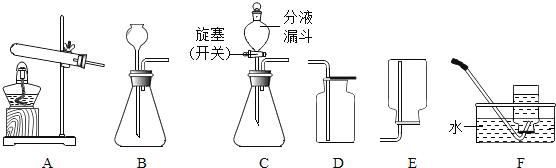
��1�������м�������Լ�a��Ϊ����������Һ������Ŀ����Ϊ�˳�ȥ�����е��� ����
��2���ڹ��˲����У����õ�����Ȧ������̨���ձ����������⣬����Ҫ�õ���������������
��3����ҺB������������Ϊ������
��4������ҺB�μ�ϡ����Ĺ����У����۲쵽����Һ������Ϊ����ʱ��Ӧֹͣ�μӣ�����μӵ�ϡ��������������õ��ľ��ξ���ijɷ�������������������û������Ӱ�졣����C������Ϊ������
��ҵ���õ�ⱥ��ʳ��ˮ�ķ�������ȡ�������ơ���������������д����Ӧ�Ļ�ѧ����ʽ�� ����
���𰸡���1���Ȼ�þ��2��©����3���Ȼ��ơ��������ƣ�̼���ƣ�4�������ݷų� û�У�5��������6��2NaCl+2H2O![]() 2NaOH+Cl2��+H2��
2NaOH+Cl2��+H2��
��������
��1����Ϊ���ζ�����ˮ�������������ӻὫþ����ת��Ϊ������þ������ʣ���Ȼ��ƣ���2������ʵ����Ҫ�õ��������У�©��������̨���ձ�������������3��ǰ��ij��Ӹ�����ʣ���Ȼ��ƣ������ڳ���ʱ������������ƺ�̼���ƣ���ȥ�Ȼ���ʱ���ù�����̼���ƣ����������Լ�b�����ǹ����ģ�
��4������ҺB�μ�ϡ���ᵱ�۲쵽��Һ�������ݷų�ʱ��ֹͣ�μӣ���ֹϡ���������������ϡ��������õ��ľ��ξ���ijɷ�û��Ӱ�죬��Ϊϡ������Ȼ��Ʒ�Ӧ����5���õ����ξ���֮ǰ�IJ�������������6���ɷ�����֪����Ӧ��������Ӧ�������ʿ���д�˻�ѧ����ʽΪ��2NaCl+2H2O![]() 2NaOH+Cl2��+H2����
2NaOH+Cl2��+H2����

 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�����Ŀ��������û����������ʱ������ˮ��������Ӧ���������£�����ˮ�����ܷ�Ӧ����һ�ֳ��������������һ�����塣С���ܺ��棬�������ʵ��̽��������ˮ������Ӧ��IJ��
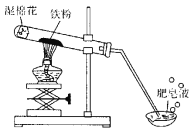
(1)�Թ�β����һ��ʪ����Ŀ����______��
(2)̽�����ɵ�������ʲô?��ȼ�ŵ�ľ�����������ݣ��б��������Ժ��з�����Ʈ�����С�˵�����ɵ�������______��
(3)̽���Թ���ʣ�����ɷ���ʲô?
���������ϣ�Fe304������ˮ���������ᷴӦ��û���������ɡ�
�������������� | FeO | Fe2O3 | Fe304 |
��ɫ��״̬ | ��ɫ��ĩ | ����ɫ��ĩ | ��ɫ���� |
�ܷ������� | �� | �� | �� |
��������֤���Թ���ʣ�����Ϊ��ɫ����ȫ��������������
����������裩����һ��ʣ�������Fe��Fe3O4��
�������ʣ�������______��
��ʵ��̽����
ʵ����� | ʵ�������� |
ȡ������ɫ�������Թ��У�����������ϡ���ᡣ | ����ȫ���ܽ⣬����û��______������˵������������� |
��ʵ����ۣ�����ˮ������Ӧ�Ļ�ѧ����ʽΪ______��
����˼�뽻�����ú�ɫ���岻������Fe2O3��������______��
����Ŀ�����б��ٲ������б�������������Ψһ���ϵ̲���ı��ǵ̵������ǵijɷ���CaCO3�������ɷּȲ�����ˮҲ�������ᷴӦ����ij��ȤС��Ϊ�˲ⶨ�ñ�����Ʒ��̼��Ƶ�������������һ�����ı�����Ʒ�����ձ��У��ٽ�100gϡ�����4�μ����ձ��У�ÿ�ξ���ַ�Ӧ��ʵ�����ݼ�¼�����
���� | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
����ϡ���������/g | 25 | 25 | 25 | 25 |
��Ӧ���ձ������ʵ�������/g | 36.4 | 59.6 | 83.8 | 108.8 |
��1����1�μ���ϡ�����ַ�Ӧ�����ɶ�����̼��������______g��
��2���ñ�����Ʒ��̼��Ƶ�����____
����Ŀ��ʵ���ҳ��ü����������������̻����ķ�����ȡ������д����Ӧ�Ļ�ѧ����ʽ��______��
С�����֣������������ͭ��ϼ��ȣ�Ҳ�ܽϿ�������������ǽ�������̽����
��������룩��MnO2�⡢CuOҲ������KClO3�ֽ�Ĵ�����
�����ʵ�飩���±�����ʵ�飺�ⶨ�ֽ��¶ȣ��ֽ��¶�Խ�ͣ���Ч��Խ�ã��棩
ʵ���� | ʵ��ҩƷ | �ֽ��¶ȣ��棩 |
�� | KClO3 | 580 |
�� | KClO3��MnO2��������1��1�� | 350 |
�� | KClO3��CuO��������1��1�� | 370 |
�� | KClO3��MnO2��������1��3�� | 320 |
���������ݡ��ó����ۣ�
��1����ʵ��______�ĶԱȣ�֤�����������
��2���Ա�ʵ��٢ڢ���ó�����ʶ��______��
����˼��
��1����Ҫ֤��CuO�Ǹ÷�Ӧ�Ĵ�������Ҫ��֤���ڻ�ѧ��Ӧǰ��������______���䣻
��2��ͬ�ִ�����������С����Ӱ���Ч���������ʵ�鷽��������֤______��