��Ŀ����
����Ŀ�������г������ʵ����ʡ��Ʒ��ǻ�ѧ�о�����Ҫ���ݡ�
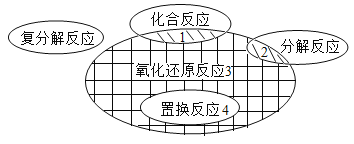
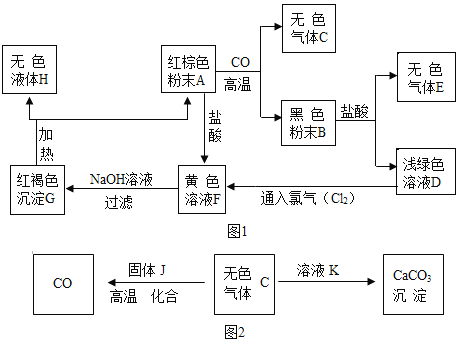
��1�����ֽⷴӦ������������_____��
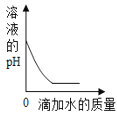
��2��m������������һ������ϡ����ǡ����ȫ��Ӧ�������õ���������������ȥ�к���ͬ��ϡ���ᣬ����Һ��pH_____7��������ڡ����ڻ�С�ڣ�
��3���������Ƴ��ڷŵ������л���ʣ���д���������Ʊ��ʵĻ�ѧ��Ӧ����ʽ_____��
��4����ͼװ�ÿ���һ����̼��ԭ��������ʵ�顣

��Ӳ���Թܢ��е�ʵ������Ϊ_____��
�ڸ�ʵ���з������Ϸ�Ӧ�Ļ�ѧ����ʽΪ_____��
�۹�ҵ���ø�¯�����������¯�м�������ʯ����̿��ʯ��ʯ�������������������ô��¯����ʱ��̿������Ϊ��_____��_____
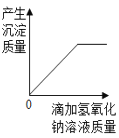
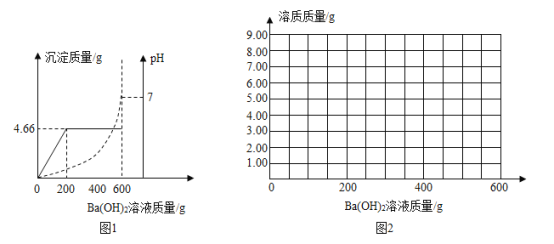
��5����ʵ���ҳ�ȡ20g��������Ʒ�����ձ��У����ʲ��μӷ�Ӧ��������100g������������Ϊ21.9%�����ᣬ����ǡ����ȫ��Ӧ���Լ�����Ʒ������������������_____��
���𰸡���Ӧ��������ӽ���������ˮ�������������Ҹ�Ԫ�صĻ��ϼ۲��� �� CO2��2NaOH=Na2CO3��H2O ����ɫ������ɫ 2CO��O2![]() 2CO2 ̼ȼ��ʱ�����������ȣ�Ϊ��Ӧ�ṩ�������� ̼���������̼���巴Ӧ�������л�ԭ�Ե�����һ����̼�����ڻ�ԭ������ 80%
2CO2 ̼ȼ��ʱ�����������ȣ�Ϊ��Ӧ�ṩ�������� ̼���������̼���巴Ӧ�������л�ԭ�Ե�����һ����̼�����ڻ�ԭ������ 80%
��������
��1�����ֽⷴӦ�����������ǣ���������������ۣ���Ӧ��������ӽ���������ˮ�������������Ҹ�Ԫ�صĻ��ϼ۲��䣻
��2��80���������������ƺ�73�������Ȼ���ǡ����ȫ��Ӧ��74���������������ƺ�73�������Ȼ���ǡ����ȫ��Ӧ��m������������һ������ϡ����ǡ����ȫ��Ӧ�������õ���������������ȥ�к���ͬ��ϡ���ᣬ����Һ�л�ʣ�����������ӣ���Һ�Լ��ԣ�pH��7��
��3���������Ƴ��ڷŵ������л���ʣ����������������̼��Ӧ����̼���ƺ�ˮ��ѧ��Ӧ����ʽ��CO2��2NaOH=Na2CO3��H2O��
��4��
��Ӳ���Թܢ���һ����̼�����������������·�Ӧ�������Ͷ�����̼���壬��ʵ������Ϊ����ɫ������ɫ��
�ڸ�ʵ����һ����̼��������ȼ�ղ���������̼�Ļ�ѧ����ʽΪ��2CO��O2![]() 2CO2���÷�Ӧ���ϡ����һ�����ڻ��Ϸ�Ӧ��
2CO2���÷�Ӧ���ϡ����һ�����ڻ��Ϸ�Ӧ��
�۹�ҵ���ø�¯�����������¯�м�������ʯ����̿��ʯ��ʯ�������������������ô��¯����ʱ��̿������Ϊ��1��̼ȼ��ʱ�����������ȣ�Ϊ��Ӧ�ṩ����������2��̼���������̼���巴Ӧ�������л�ԭ�Ե�����һ����̼�����ڻ�ԭ��������
��5���⣺����Ʒ��������������Ϊx��

![]() x=16g
x=16g
��Ʒ������������������=![]() ��
��

����Ŀ��������۩��۩�������֮�佨����ϵ����ѧϰ��ѧ��һ����Ҫ��˼ά��ʽ����ͼ��Ԫ�����ڱ��в���Ԫ�ص�ԭ�ӽṹʾ��ͼ��������ѧ֪ʶ�ش����е����⣮
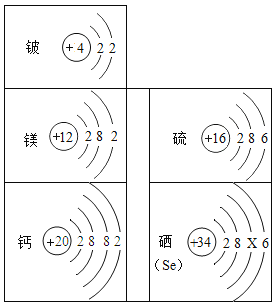
��1����ԭ�ӽṹʾ��ͼ�е�X=____����Ԫ������______�����������������ǽ�������Ԫ�أ�
��2��Ӳˮ�к��еĽ�������Ϊ________�������ӷ��ţ���
��3����Ԫ�غ���Ԫ�صĻ�ѧ�������ƣ���������Ļ�ѧʽΪ________��
��4����Է����������״���µ��������֮����ڽ��ܵĹ�ϵ�����±����������±��жϣ���״����22.4L����������YΪ______��������±����ɳ�һ�����ɣ�______��
���� | ���� | ���� | |
��Է������� | 2 | 32 | 28 |
��״���£�22.4L��������� | 2g | 32g | Y |