题目内容
用100g稀硫酸跟一定质量的锌恰好完全反应,生成了0.4g氢气,计算:
(1)稀硫酸中硫酸的质量分数;
(2)反应后所得溶液中溶质的质量分数.
(3)若50g这种稀硫酸稀释成10%;需加入多少克水?
解:设硫酸的质量为x,硫酸锌的质量为y,
Zn+H2SO4=ZnSO4+H2↑
98 161 2
x y 0.4g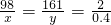 x=19.6g y=32.2g
x=19.6g y=32.2g
稀硫酸中硫酸的质量分数=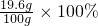 =19.6%;
=19.6%;
反应后所得溶液中溶质的质量分数=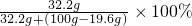 =28.6%
=28.6%
设加水的质量为z
50g×19.6%=(50g+z)×10% z=48g
故答案为:(1)19.6%(2)28.6%(3)48g
分析:根据化学方程式计算的步骤有:一设、二写、三找、四列、五答、六查.在本题中,根据氢气的质量可以求硫酸和硫酸锌的质量,再根据溶质的质量分数公式求稀硫酸和硫酸锌溶液的质量分数;溶液的稀释问题,要记住溶质的质量不变.
点评:本考点考查了根据化学方程式的计算和溶液的稀释问题,属于质量分数和化学方程式的综合应用,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,还要记牢质量分数的公式.本考点主要出现在计算题中.
Zn+H2SO4=ZnSO4+H2↑
98 161 2
x y 0.4g
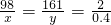 x=19.6g y=32.2g
x=19.6g y=32.2g稀硫酸中硫酸的质量分数=
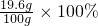 =19.6%;
=19.6%;反应后所得溶液中溶质的质量分数=
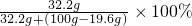 =28.6%
=28.6%设加水的质量为z
50g×19.6%=(50g+z)×10% z=48g
故答案为:(1)19.6%(2)28.6%(3)48g
分析:根据化学方程式计算的步骤有:一设、二写、三找、四列、五答、六查.在本题中,根据氢气的质量可以求硫酸和硫酸锌的质量,再根据溶质的质量分数公式求稀硫酸和硫酸锌溶液的质量分数;溶液的稀释问题,要记住溶质的质量不变.
点评:本考点考查了根据化学方程式的计算和溶液的稀释问题,属于质量分数和化学方程式的综合应用,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律,还要记牢质量分数的公式.本考点主要出现在计算题中.

练习册系列答案
 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
在课堂中,同学们用硫酸、硝酸钡、氢氧化钠、碳酸钾四种物质的溶液,进行复分解反应发生条件的探究.
(1)通过判断上述四种溶液两两之间能否发生反应,写出其中符合下列条件的化学方程式.
有沉淀生成的反应:______.
(2)下面图1是HCl和NaOH在水中解离的微观示意图;图2是稀盐酸和氢氧化钠反应的微观过程示意图.
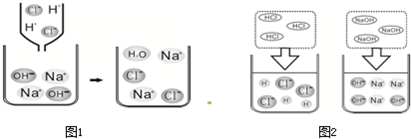
①盐酸和氢氧化钠发生反应的微观实质是什么?______.
②通过课堂上的探究能发现:在溶液中,除了H+和OH-不能大量共存外,______(填两种离子符号)也不能大量共存.
(3)利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液.
①经测定,该溶液显酸性.则该溶液中一定含有的离子是______.(至少写4种离子符号)
②为验证该溶液中可能含有的离子是否存在,我设计如下实验进行验证.(验证一种离子即可)
| 溶液中可能含有的离子 | 设计实验验证(实验步骤、现象及对应的结论) |
| ______ | ______ |
在课堂中,同学们用硫酸、硝酸钡、氢氧化钠、碳酸钾四种物质的溶液,进行复分解反应发生条件的探究.
(1)通过判断上述四种溶液两两之间能否发生反应,写出其中符合下列条件的化学方程式.
有沉淀生成的反应:______.
(2)下面图1是HCl和NaOH在水中解离的微观示意图;图2是稀盐酸和氢氧化钠反应的微观过程示意图.
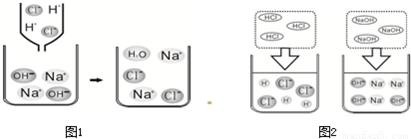
①盐酸和氢氧化钠发生反应的微观实质是什么?______.
②通过课堂上的探究能发现:在溶液中,除了H+和OH-不能大量共存外,______(填两种离子符号)也不能大量共存.
(3)利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液.
①经测定,该溶液显酸性.则该溶液中一定含有的离子是______.(至少写4种离子符号)
②为验证该溶液中可能含有的离子是否存在,我设计如下实验进行验证.(验证一种离子即可)
(4)100g稀盐酸恰好跟100g溶质质量分数为16%的氢氧化钠溶液完全反应,求所得溶液中溶质的质量分数.
(1)通过判断上述四种溶液两两之间能否发生反应,写出其中符合下列条件的化学方程式.
有沉淀生成的反应:______.
(2)下面图1是HCl和NaOH在水中解离的微观示意图;图2是稀盐酸和氢氧化钠反应的微观过程示意图.

①盐酸和氢氧化钠发生反应的微观实质是什么?______.
②通过课堂上的探究能发现:在溶液中,除了H+和OH-不能大量共存外,______(填两种离子符号)也不能大量共存.
(3)利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液.
①经测定,该溶液显酸性.则该溶液中一定含有的离子是______.(至少写4种离子符号)
②为验证该溶液中可能含有的离子是否存在,我设计如下实验进行验证.(验证一种离子即可)
| 溶液中可能含有的离子 | 设计实验验证(实验步骤、现象及对应的结论) |
| ______ | ______ |
