题目内容
【题目】有一包白色固体样品,可能由硫酸钠,硝酸铵,碳酸钙,氯化镁,氯化钡中的一种或者几种组成,为了探究该样品的组成,某兴趣小组同学取适量样品,按下列流程进行实验(假设各步反应均恰好完全进行)
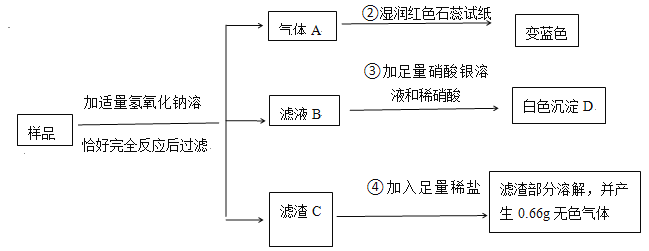
请你填空:
(1)产生的气体A为___________,白色沉淀D为___________(填写化学式,下同)
(2)滤渣C中一定含有的物质是___________
(3)根据上述实验推测,样品的组成可能有___________种情况。
【答案】 NH3 AgCl CaCO3和BaSO4 2
【解析】本题推断题。在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可。
铵盐能与氢氧化钠反应能生成氨气,氨气能使湿润红色石蕊试纸变蓝色。样品中的物质与氢氧化钠反应生成能使湿润红色石蕊试纸变蓝色的气体,说明生成有气体是氨气,样品中含有铵根,所以样品中一定存在硝酸铵;硝酸银溶液与含有氯离子的盐反应能生成氯化银的白色沉淀,氯化银不溶于稀硝酸。样品与氢氧化钠反应后的滤液与足量的硝酸银溶液和稀硝酸混合产生了白色沉淀,白色沉淀是氯化银,滤液中存在氯离子,所以样品中存在氯化镁,氯化钡中一种或两种;碳酸钙能与稀盐酸反应生成二氧化碳气体,硫酸钠与氯化钡能生成不溶于稀盐酸的白色沉淀。滤渣C加入足量稀盐酸,滤渣部分溶解,并产生气体,说明滤渣中一定碳酸钙和硫酸钡,所以样品中一定存在硫酸钠、氯化钡和碳酸钙,综上所述,样品中一定含有硫酸钠、硝酸铵、碳酸钙、氯化钡,可能含有氯化镁。因此:
(1)产生的气体A为氨气,化学式是NH3;白色沉淀D为氯化银,化学式是AgCl;
(2)滤渣C中一定含有的物质是CaCO3和BaSO4;
(3)根据上述实验推测,样品中一定含有硫酸钠、硝酸铵、碳酸钙、氯化钡,可能含有氯化镁,样品的组成可能有2种情况。

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案【题目】溶液在生产、生活中起着十分重要的作用。
(1)可作为溶质的是_______。
A.只有固体 B. 只有液体
C.只有气体 D. 气体、液体、固体都可以
(2)物质加入足量水中,能形成无色透明溶液的是_______。
A.汽油 B. 面粉 C. 纯碱 D. 硫酸铜
(3)物质加入水中形成溶液过程中,温度会升高的是_______。
A.烧碱 B. 氯化钠 D. 氧化钙 D. 碳酸钙
(4)下表是NaCl和KNO3在不同温度时的溶解度,回答问题。
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度g/100g水 | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |
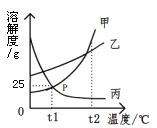
①两种物质中,溶解度受温度影响变化较大的是__________。
②NaCl和KNO3溶解度相等的温度范围是__________。
③KNO3晶体中含有少量NaCl,提纯KNO3晶体的方法是__________。
④60℃时,按图示操作:
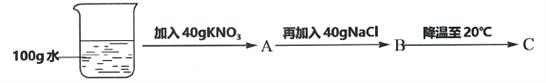
A中溶液是__________(填“饱和”或“不饱和”)溶液,C中溶液的总质量是__________g。
⑤50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:NaCl溶液__________(填“大于”“等于”或“小于”)KNO3溶液。