题目内容
 请按要求填空:
请按要求填空:(1)地壳中含量最多的非金属元素是
(2)常用于治疗胃酸过多的碱的化学式
(3)t℃时,5.2g KNO3固体溶于20.0g水中,刚好形成饱和溶液.t℃时,KNO3的溶解度为
(4)久置在空气中的氢氧化钠溶液,会生成一种盐类杂质,向其中加入稀盐酸时会产生无色气体.生成这种杂质的化学方程式为:
(5)某简单粒子的结构示意图如图:
当x=8时,该粒子符号为
当x=10时,该粒子符号为
当x=13时,写出该粒子的盐酸盐的化学式为:
考点:地壳中元素的分布与含量,固体溶解度的概念,碱的化学性质,盐的化学性质,原子结构示意图与离子结构示意图,化学式的书写及意义
专题:物质的微观构成与物质的宏观组成,化学用语和质量守恒定律,溶液、浊液与溶解度
分析:(1)根据地壳中各元素含量的排序及化学式的书写方法进行分析判断.
(2)胃液的主要成分是盐酸,可以服用能与盐酸反应的物质来治疗胃酸过多,同时又不能伤害身体.
(3)根据溶解度的概念进行分析,溶解度就是在一定温度下,某物质在100g水中达到饱和时溶解的质量.
(4)根据氢氧化钠变质是二氧化碳与氢氧化钠反应生成碳酸钠和水,碳酸钠与盐酸反应生成氯化钠、水、二氧化碳,根据碳酸钠、氢氧化钠都是显碱性,能使酚酞试液变红.
(5)根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;据此进行分析解答.
(2)胃液的主要成分是盐酸,可以服用能与盐酸反应的物质来治疗胃酸过多,同时又不能伤害身体.
(3)根据溶解度的概念进行分析,溶解度就是在一定温度下,某物质在100g水中达到饱和时溶解的质量.
(4)根据氢氧化钠变质是二氧化碳与氢氧化钠反应生成碳酸钠和水,碳酸钠与盐酸反应生成氯化钠、水、二氧化碳,根据碳酸钠、氢氧化钠都是显碱性,能使酚酞试液变红.
(5)根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;据此进行分析解答.
解答:解:(1)地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,其中含量最多的非金属元素是氧元素.空气的成分按体积计算,大约是:氮气占78%、氧气占21%,空气中含量最多的气体是氮气.故答案为:氧;N2.
(2)氢氧化铝可以与盐酸反应生成氯化铝和水,能用于治疗胃酸过多,还具有胃粘膜保护作用,故填:Al(OH)3.
(3)2t℃时,将5.2gKNO3固体溶于20.0g水中刚好形成饱和溶液,则此时硝酸钾的溶解度是
×100g=26.0g,故填:26.0g;
(4)碳酸钠与盐酸反应生成氯化钠、水、二氧化碳,所以这种无色气体是二氧化碳;氢氧化钠变质的反应物是二氧化碳和氢氧化钠写在等号的左边,生成物是碳酸钠和水写在等号的右边,用观察法配平,所以方程式是:CO2+2NaOH═Na2CO3+H2O;因为碳酸钠溶液显碱性,氢氧化钠属于碱都能使酚酞试液变为红色.
故答案为:CO2+2NaOH═Na2CO3+H2O;红.
(5)解:某简单粒子的结构示意图如图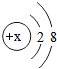 所示,当x=8时,质子数=8,核外电子数=10,质子数<核外电子数,为带2个单位负电荷的氧离子,其离子符号为O2-.
所示,当x=8时,质子数=8,核外电子数=10,质子数<核外电子数,为带2个单位负电荷的氧离子,其离子符号为O2-.
当x=10时,质子数=核外电子数=10,为氖原子,其原子符号为:Ne.
当x=13时,质子数=13,核外电子数=10,质子数>核外电子数,为带3个单位负电荷的铝离子;该粒子的盐酸盐为氯化铝,铝元素显+3价,氯显-1价,其化学式为:AlCl3.
故答案为:O2-;Ne;AlCl3.
(2)氢氧化铝可以与盐酸反应生成氯化铝和水,能用于治疗胃酸过多,还具有胃粘膜保护作用,故填:Al(OH)3.
(3)2t℃时,将5.2gKNO3固体溶于20.0g水中刚好形成饱和溶液,则此时硝酸钾的溶解度是
| 5.2g |
| 20.0g |
(4)碳酸钠与盐酸反应生成氯化钠、水、二氧化碳,所以这种无色气体是二氧化碳;氢氧化钠变质的反应物是二氧化碳和氢氧化钠写在等号的左边,生成物是碳酸钠和水写在等号的右边,用观察法配平,所以方程式是:CO2+2NaOH═Na2CO3+H2O;因为碳酸钠溶液显碱性,氢氧化钠属于碱都能使酚酞试液变为红色.
故答案为:CO2+2NaOH═Na2CO3+H2O;红.
(5)解:某简单粒子的结构示意图如图
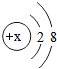 所示,当x=8时,质子数=8,核外电子数=10,质子数<核外电子数,为带2个单位负电荷的氧离子,其离子符号为O2-.
所示,当x=8时,质子数=8,核外电子数=10,质子数<核外电子数,为带2个单位负电荷的氧离子,其离子符号为O2-.当x=10时,质子数=核外电子数=10,为氖原子,其原子符号为:Ne.
当x=13时,质子数=13,核外电子数=10,质子数>核外电子数,为带3个单位负电荷的铝离子;该粒子的盐酸盐为氯化铝,铝元素显+3价,氯显-1价,其化学式为:AlCl3.
故答案为:O2-;Ne;AlCl3.
点评:本题考查了有关溶解度的概念、地壳中元素含量、二氧化碳的化学性质等,完成此题,可以依据已有的概念进行.

练习册系列答案
相关题目
黄金是一种贵重金属,在人类漫长的历史中,素有“沙里淘金”、“真金不怕火炼”之说.下列关于黄金的说法中,不正确的是( )
| A、黄金在自然界中是以单质的形式存在的 |
| B、黄金的化学性质非常稳定 |
| C、黄金作为贵重金属,是因为他非常稀少 |
| D、黄金是合金的一种 |