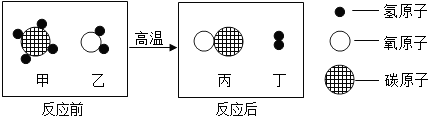
题目内容
生活中处处有化学,金属在日常生活中用途广泛:
(1)铝箔包装药物,主要利用了铝的 性;
(2)铜具有很好的 性,故可作导线,但长期露置于空气中,铜制品会和空气中的O2、H2O及 会生成铜锈[Cu2(OH)2CO3];
(3)用铁锅烹饪食物时,会有少量铁屑在胃部转化为可被吸收的Fe2+,反应的化学方程式为 ,是 反应(填基本反应类型).
(1)铝箔包装药物,主要利用了铝的
(2)铜具有很好的
(3)用铁锅烹饪食物时,会有少量铁屑在胃部转化为可被吸收的Fe2+,反应的化学方程式为
考点:金属的物理性质及用途,金属的化学性质,金属锈蚀的条件及其防护,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)利用铝的延展性来回答;
(2)根据铜的导电性,与氧气、水、二氧化碳的反应进行分析;
(3)根据胃酸与铁的反应及反应类型进行分析.
(2)根据铜的导电性,与氧气、水、二氧化碳的反应进行分析;
(3)根据胃酸与铁的反应及反应类型进行分析.
解答:解:(1)因为铝具有良好的延展性,可以用来制作包装食品或药品用的铝箔;
(2)根据铜具有很好的导电性,铜生锈是铜与水、氧气和二氧化碳共同作用的结果;
(3)胃中含有胃酸,胃酸主要是盐酸,盐酸与铁反应可以生成FeCl2,这样少量铁屑在胃部转化为可被吸收的Fe2+,反应方程式是:Fe+2HCl═FeCl2+H2↑;属于置换反应.
故答案为:(1)延展;(2)导电;CO2;(3)Fe+2HCl═FeCl2+H2↑;置换.
(2)根据铜具有很好的导电性,铜生锈是铜与水、氧气和二氧化碳共同作用的结果;
(3)胃中含有胃酸,胃酸主要是盐酸,盐酸与铁反应可以生成FeCl2,这样少量铁屑在胃部转化为可被吸收的Fe2+,反应方程式是:Fe+2HCl═FeCl2+H2↑;属于置换反应.
故答案为:(1)延展;(2)导电;CO2;(3)Fe+2HCl═FeCl2+H2↑;置换.
点评:本题主要考查金属的物理性质和化学性质,掌握金属的性质及用途是正确解答本题的关键.

练习册系列答案
相关题目
下列叙述中属于物理变化的是( )
| A、氧气在一定的条件下能够变成液态的形式 |
| B、氧气在一定条件下转变成液态形式 |
| C、铁在潮湿的空气中能够有铁锈生成 |
| D、铁在潮湿的空气中有铁锈生成 |
下列实验操作正确的是( )
A、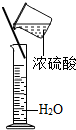 稀释浓硫酸 |
B、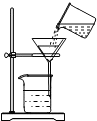 过滤 |
C、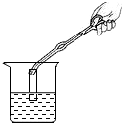 检测溶液的pH |
D、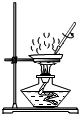 蒸发 |
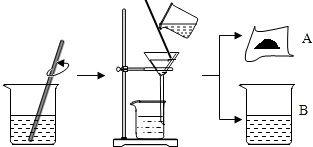 将贝壳(主要成分是碳酸钙)灼烧后与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.某化学学习小组的同学们为了制取氢氧化钾,将少量碳酸钙充分灼烧后的固体放入烧杯中,再向其中加入一定量10%的碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B.操作步骤如图所示.小组同学对固体A、溶液B进行如下猜想与探究:
将贝壳(主要成分是碳酸钙)灼烧后与草木灰(主要成分是碳酸钾)在水中作用,可以得到氢氧化钾.某化学学习小组的同学们为了制取氢氧化钾,将少量碳酸钙充分灼烧后的固体放入烧杯中,再向其中加入一定量10%的碳酸钾溶液,充分反应冷却后过滤、洗涤得到固体A和溶液B.操作步骤如图所示.小组同学对固体A、溶液B进行如下猜想与探究: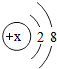 请按要求填空:
请按要求填空: