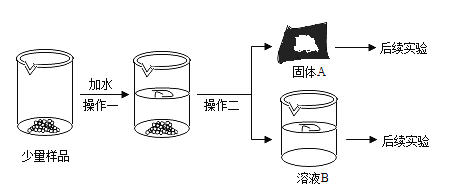
题目内容
【题目】我国的煤炭资源丰富,但液体燃料短缺。通过“煤液化”技术,用煤炭和水制取甲醇(CH3OH)对我国具有重要意义。主要流程如图:
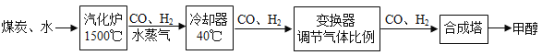
(1)投入汽化炉中的煤炭粉碎的目的是_____。
(2)汽化炉中发生的化学方程式是_____。
(3)为了提高原料的利用率,变换器中应控制合成气体积之比为:V(CO):V(H2)=_____。
(4)利用CO、H2还可以合成多种物质。仅用CO、H2为原料不可能得到的物质是_____。
①乙醇(C2H6O) ②尿素(CO(NH2)2) ③甲醛(CH6O)
(5)“煤液化”相对于传统的“燃煤”的优点是_____。
【答案】增大反应的接触面积,使反应更充分  1:2 ①② 减少大气污染物的排放(或提高了能源的利用率)
1:2 ①② 减少大气污染物的排放(或提高了能源的利用率)
【解析】
(1)投入汽化炉中的煤炭粉碎的目的是增大反应的接触面积,使反应更充分。故填:增大反应的接触面积,使反应更充分;
(2)汽化炉中碳和水蒸气在高温条件下反应,生成一氧化碳和氢气,发生的化学方程式是: 。故填:
。故填: ;
;
(3)合成甲醇的方程式为CO+2H2→CH3OH,由方程式可知上述工艺中应控制合成气中V(CO):V(H2)=1:2,故填:1:2;
(4)由质量守恒定律可知化学反应前后元素的种类不变,可知反应前元素有三种即碳氢氧,反应后不会出现氮元素,所以尿素不可能产生;根据碳原子与氧原子个数比可知,①也不可能,故填:①②;
(5)“煤液化”相对于传统的“燃煤”的优点是减少大气污染物的排放(或提高了能源的利用率)。故填:减少大气污染物的排放(或提高了能源的利用率)。

【题目】某些铜制品在空气中久置。表面生成绿色的铜锈(又称铜绿)。某化学实验小组设计并进行实验,探究铜锈的组成和铜生锈的条件。
I.探究铜锈的组成
[查阅资料]①铜锈受热易分解 ②硫酸铜粉末遇水由白色变为蓝色
[进行实验]小组同学从铜器上取下适量的干燥铜锈,按如图所示装置实验(部分夹持装置已略去)。观察到B中白色粉末变为蓝色,C中澄清石灰水变浑浊。

[解释与结论](1)依据以上现象分析,铜锈中一定含有的元素: Cu、O、_____
II.探究铜生锈的条件
[提出猜想]根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
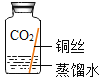
[进行实验]实验小组同学取直径、长度均相同的铜丝,并打磨光亮。设计了如下图所示的5个实验并持续观察。
编号 | ① | ② | ③ | ④ | ⑤ |
实验 |
|
|
|
|
|
现象 | 无明显现象 | 无明显现象 | 铜丝表面有绿色物质 | 无明显现象 | 无明显现象 |
[解释与结论]
(2)得出“铜生锈一定与CO2有关”的结论,依据的两个实验是_____(填编号)。
(3)对比实验②和③,得出的结论是_____。
(4)为验证猜想,请在图中将实验⑤补充完整。补充的物质应为_____。
(5)由上述实验可推知,铜生锈的条件是_____。
【题目】铁、铝、铜是常见的三种金属。同学们发现生活中的铝和铜制品表面一般不用防锈,而铁制品一般需要做防锈处理。
(1)提出问题:这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
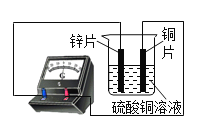
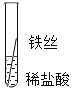
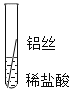
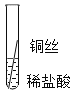
(2)实验探究:同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格将粗细相同的铁丝、铝丝、铜丝分别插人体积相同、溶质质量分数也相冋的稀盐酸中:
操作 |
|
|
| 根据现象得出金属活动性顺序 |
片刻后现象 | 有少量气泡 | 无气泡 | 无气泡 | Fe>Al, Fe>Cu |
几分钟后现象 | 有少量气泡 | 有大量气泡 | 无气泡 | _____ |
(3)讨论交流:为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表面致密的氧化膜会先与盐酸反应。
(4)反思评价:做金属性质实验时需将金属进行打磨,打磨的目的是_____。
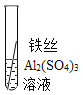
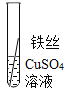
(5)实验验证:为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
操作 |
|
| 根据现象得出金属活动性顺序 |
现象 | 无明显现象 | _____ | Al>Fe>Cu |
写出铁与硫酸铜溶液反应的化学反应方程式_____。
(6)拓展迁移:若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插入顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序。金属丝的插入顺序为_____。
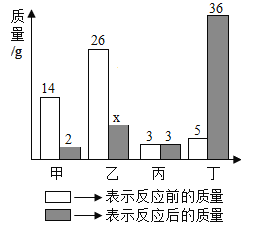
【题目】某实验小组的同学为了测定实验室中高锰酸钾样品的纯度,取20g该样品,依次加热该混合物,t1、t2、t3、t4时间后,称得剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应)
加热时间 | t1 | t2 | t3 | t4 |
剩余固体质量(g) | 19.88 | 19.56 | 19.36 | 19.36 |
试计算:(1)加热__________时间后高锰酸钾已经完全反应。
(2)完全反应后产生氧气的质量为_________g。
(3)求该样品中高锰酸钾的质量分数_______。
【题目】已知某种铸造钢轨的金属粉末原料中可能含有铁、锰、铜三种金属中的两种或三种,化学小组的同学对该粉末进行探究
(1)提出猜想:
猜想Ⅰ:该粉末由铜、锰组成
猜想Ⅱ:该粉末由铁、锰组成
猜想Ⅲ:1该粉末由铁、锰、铜组成
猜想Ⅳ:该粉末由____________组成。
(2)查阅资料:金属锰、铜不能被磁铁吸引,锰和硫酸亚铁溶液可以发生置换反应锰元素在生成物中显+2价,生成物的溶液为浅粉色。
(3)进行实验
实验目的 | 实验操作 | 实验现象 |
①证明粉末中是否含有铜 | 取一个小烧杯,加入适量的粉末,再向其中加入过量的___________。 | 有少量红色粉末不能溶解 |
②证明粉末中是否含有锰 | 取5.5g的粉末放入烧杯,再向其中加入过量的硫酸亚铁溶液,反应完全后过滤、干燥、称量固体为5.52g | _____ |
③证明粉末中是否含有铁 | 另取5.5g粉末___________(用物理方法),剩余金属粉末的质量为1.12g | _____ |
(4)初步结论:猜想_______成立,写出实验①中发生反应的一个化学反应方程式为_________________。
(5)数据处理:试计算粉末原料中任意一种金属所占的质量分数____________(用金属的名称和百分数表示,结果保留一位小数)。