题目内容
【题目】请结合下图回答问题:

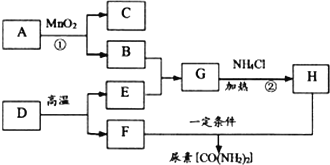
(1)仪器名称:①_______,②_______。
(2)用氯酸钾制取氧气,可选用的发生装置是______(选填序号),该反应的化学方程式为______。用D装置收集氧气完毕后,应先______(选填“从水中取出导管”或“熄灭酒精灯”)。
(3)实验室制取CO2,反应的化学方程式为______,为方便控制反应的发生和停止,应选择的发生装置是_____(选填序号),可用C装置收集CO2的理由是______。
(4)如图是某学生设计的一种由洗气、除杂、检验等用途的装置,当用排水法收集氢气时,瓶内先装满水,气体从_____(选填“a”或“b”),用该装置还可以检验CO2,写出发生反应的化学方程式_______。
【答案】长颈漏斗 水槽 A ![]() 从水中取出导管 CaCO3+2HCl==CaCl2+H2O+CO2↑ F CO2密度比空气大 b CO2+Ca(OH)2==CaCO3↓+H2O
从水中取出导管 CaCO3+2HCl==CaCl2+H2O+CO2↑ F CO2密度比空气大 b CO2+Ca(OH)2==CaCO3↓+H2O
【解析】
(1)长颈漏斗方便加液体药品,水槽是盛水的仪器,仪器名称①长颈漏斗;②水槽。
(2)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,化学方程式为:![]() ;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;
;实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,化学方程式为:CaCO3+2HCl==CaCl2+H2O+CO2↑,因此不需要加热。二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;F装置可以控制反应的发生和停止;
(4)当用排水法收集氢气时,瓶内先装满水,气体从短管进入,因为氢气的密度比水小;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳;化学方程式为:CO2+Ca(OH)2==CaCO3↓+H2O。

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案【题目】如图为采用“数字化”实验,由传感器采集实验相关信息描绘出曲线,其中物质X表示能与二氧化碳反应的某溶液,纵坐标y表示烧杯中的某个量。下列对物质X与纵坐标y的分析正确的是
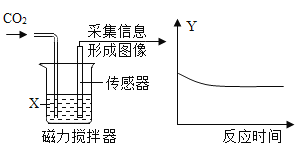
选项 | 物质X | 纵坐标y |
A | 水 | 溶液的质量 |
B | 水 | 溶液的pH |
C | 氢氧化钠溶液 | 溶质的质量 |
D | 氢氧化钙溶液 | 溶液中钙元素质量 |
A. AB. BC. CD. D
【题目】清洁、高效的能源日益受到人们的重视。
(1)一氧化碳、氢气、甲烷三种气体可成为理想的燃料是____。
表1一定质量的燃料完全燃烧放出的热量
燃料 | 一氧化碳 | 氢气 | 甲烷 |
质量 | 28g | 2g | 16g |
热量(kJ) | 283.0 | 285.8 | 890.3 |
①写出一氧化碳燃烧的化学方程式________________。
②比较等质量表1中的燃料完全燃烧,放出热量最多的是_____。
(2)在红热的炭上洒少量水,炉火会烧得更旺,这是因为红热的炭能与水蒸气反应生成两种具有可燃性的气体,这两种气体是水煤气的主要成分。请写出该反应的化学方程式:____________。
【题目】某化学兴趣小组在实验室用氯酸钾和二氧化锰混合加热制备氧气,该反应的化学方程式为_______。但实验中发现制得的气体有刺激性气味,于是在老师的指导下对该气体成分进行探究。
(提出问题)刺激性气味的气体是什么呢?
(猜想与假设)
猜想一:该气体为臭氧(O3);猜想二:该气体为HCl;猜想三:该气体为Cl2
同学们认为不需要验证就可以判断猜想_____是错误的。理由是_____
(查阅资料)
(1)Cl2 +H2O=HCl +HClO;
(2)HCl +AgNO3=AgCl(白)↓ + HNO3;
(3)HClO具有强氧化性和漂白性,使有色物质褪色;
(4)臭氧在二氧化锰存在的情况下极易分解产生氧气。
(实验探究)
查阅资料后大家认为猜想一是错误的,理由是______________________________
他们为了验证剩下的猜想,继续做实验:
序号 | 实验操作 | 实验现象 | 实验结论 |
1 | 取氯酸钾和二氧化锰的混合物放入试管中加 热,将蘸有硝酸银溶液的玻璃棒伸入试管口 | _________________ | 剩下的猜想正确 |
2 | 再将湿润的蓝色石蕊试纸悬于试管口 | ______________ |
(反思与拓展)
(1)自来水厂常用漂白粉杀菌消毒﹝主要成分的化学式为Ca(ClO)2﹞。在水中起杀菌消毒作用的离子是___(填离子符号)
(2)MnO2不仅能作催化剂还可以作反应物,实验室通常用MnO2与浓盐酸共热制取Cl2,同时还生成MnCl2和一种常见的液体。请完成该反应的化学方程式:_____。