题目内容
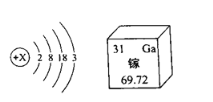
【题目】人类社会发展离不开金属材料。如图是某硬铝的主要成分。

(1)硬铝属于_____。(填“合金”或“纯金属”)
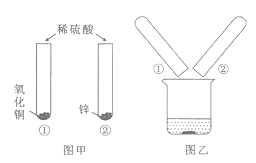
(2)将适量硬铝(已砂纸打磨处理)放入足量稀硫酸中,观察到现象为___,反应的化学方程式有______。
(3)将足量硬铝粉末放入硝酸银溶液中,充分反应后,溶液出现蓝色,出现蓝色的原因是_________,写出此时溶液中溶质成分并说明理由________。
【答案】 合金 固体部分溶解 Mg+H2SO4═MgSO4+H2↑,2Al+3H2SO4═Al2(SO4)3+3H2↑ 铜和硝酸银反应生成了易溶于水的硝酸铜 铜在三种金属中最不活泼,既然铜和硝酸银已经反应,则铝、镁都已经完全反应,因此溶质有硝酸铝、硝酸镁、硝酸铜
【解析】(1)硬铝是三种金属熔合而成的具有金属特性的物质,属于合金;(2)将适量硬铝(已砂纸打磨处理)放入足量稀硫酸中,稀硫酸和镁反应生成硫酸镁和氢气,和铝反应生成硫酸铝和氢气,不能和铜反应,因此观察到固体部分溶解,反应的化学方程式为:Mg+H2SO4═MgSO4+H2↑,2Al+3H2SO4═Al2(SO4)3+3H2↑;(3)将足量硬铝粉末放入硝酸银溶液中,充分反应后,溶液出现蓝色,出现蓝色的原因是铜和硝酸银反应生成了易溶于水的硝酸铜;铜在三种金属中最不活泼,既然铜和硝酸银已经反应,则铝、镁都已经完全反应,因为硬铝足量,则硝酸银完全反应,因此溶质有硝酸铝、硝酸镁、硝酸铜。

【题目】请从A、B两题中任选一个作答。若两题均答,按A计分。
题号 | A | B |
实验目的 | 探究_________ | 探究________ |
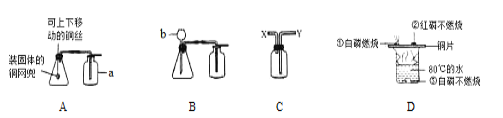
实验装置 |
|
|
实验原理 | (1)化学方程式是_______ | (1)化学方程式是_______ |
部分实验现象 | (2)溶液蓝色逐渐变浅,天平指针_______; | (2)如图,缓慢打开左端活塞,a处可观察到_______; |