题目内容
【题目】元素周期表是学习化学的重要工具。下图是元素周期表的一部分,我们对它们进行研究。
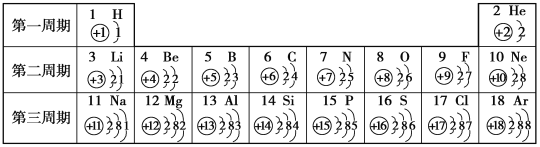
(1)第16号元素位于第_________周期,属于________(填“金属”或“非金属”)元素,它在化学反应中容易_______(填“得”或“失”)电子。
(2)科学家宣布,现已人工合成了第120号元素,则此元素的核电荷数为_____________。
(3)元素周期表中不同种元素最本质的区别是_____________。
(4)在上图中,与铍元素化学性质相似的元素为______________(写出元素符号)。
【答案】三 非金属 得 120 质子数或核电荷数不同 Mg
【解析】
(1)由元素周期表可知:第16号元素是硫元素,位于第三周期,硫元素不带“钅”字旁,属于非金属元素,硫原子最外层有6个电子,它在化学反应中容易得2个电子。
(2)科学家宣布,现已人工合成了第120号元素,则此元素的核电荷数=质子数=原子序数=120。
(3)元素是具有相同质子数或核电荷得一类原子总称,不同种元素最本质的区别是:质子数或核电荷数不同。
(4)最外层电子数相同,化学性质相似;在上图中,铍元素、镁元素的原子最外层都是2个电子,则与铍元素化学性质相似的元素为:Mg。

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目