题目内容
【题目】实验室有一瓶标签残缺且没有完全密封的无色溶液(如下图),化学兴趣小组的同学经过寻问老师,只知道原溶液是NaCl、NaOH、Na2CO3、NaHCO3中的一种溶液。

(提出问题)原瓶中是何种溶液,是否变质
(进行猜想)
猜想Ⅰ:原瓶中是NaCl溶液;
猜想Ⅱ:原瓶中是NaOH溶液;
猜想Ⅲ:原瓶中是Na2CO3溶液;
猜想Ⅳ:原瓶中是NaHCO3溶液。
(查阅资料)常温下,有关物质的相关信息如下表:
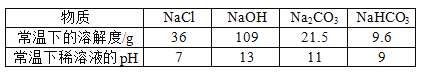
从上表可知,猜想Ⅳ一定错误,因为______。
(进行实验)(1)取少量样品,测得溶液的pH大于7,显然猜想______错误。
(2)已知:在溶液中BaCl2与NaOH不能反应,BaCO3难溶于水且能与盐酸发生反应生成CO2。同学另取样品,又进行了如下实验:
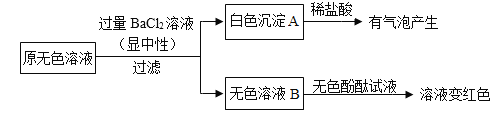
①已知生成白色沉淀A的化学反应是复分解反应,则该反应的化学方程式是______。
②通过实验可以判断,样品无色溶液中含有的溶质有______和______。
(获得结论)猜想______正确,但其中的溶质已部分变质。
(拓展延伸)实验(2)中检验无色溶液B时,能代替酚酞试液的试剂或试纸是______(填字母)。
a.金属镁 b.红色石蕊试纸 c.稀盐酸
【答案】碳酸氢钠的饱和溶液溶质质量分数在该温度下不能达到10% 猜想Ⅰ Na2CO3+CaCl2=CaCO3↓+2NaCl NaOH Na2CO3 猜想Ⅱ b
【解析】
[查阅资料]根据计算可以知道在20℃时饱和碳酸氢钠的质量分数为![]() ×100%=8.8%<10%,所以能够排除碳酸氢钠;
×100%=8.8%<10%,所以能够排除碳酸氢钠;
[进行实验](1)测定溶液的pH大于7,而氯化钠溶液呈中性,pH等于7所以不可能是氯化钠;
(2)①过量的氯化钙可以检验并除尽碳酸钠,碳酸钠可以和氯化钙反应生成碳酸钙沉淀和氯化钠,产生白色沉淀的化学方程式是Na2CO3+CaCl2=CaCO3↓+2NaCl;
②滴加无色酚酞,滤液变红,说明溶液呈碱性,还有氢氧化钠,实验可以判断原无色溶液中含有的溶质有:NaOH、Na2CO3;
[获得结论]该瓶原来装的无色溶液的溶质是NaOH,并且部分变质;
[拓展延伸]实验(2)中检验无色溶液B时,能代替酚酞试液的试剂或试纸是红色石蕊试纸。