��Ŀ����
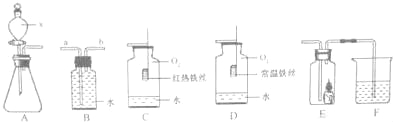
����Ŀ����ͼ A��B��C �������о�������ɵ�ʵ�飬���о�������֪��
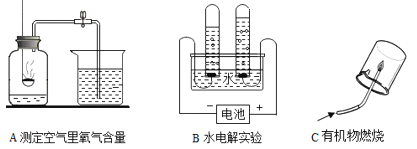
��1��A ʵ�������ÿ�ȼ���������ƿ�ڵ�����ʹƿ��ѹǿ��С���Ʋ�����������ĺ� ������Ӧ�Ļ�ѧ����ʽΪ___��
��2��B ʵ��õ�ˮ������Ԫ�غ���Ԫ����ɵĽ��ۣ�����������___��
��3��C ʵ���ͨ������ȼ�ղ����ƶϿ�ȼ����ɣ��罫 1.5g ij�л��������ڿ����г��ȼ�գ��ⶨ������ 4.4g ������̼�� 2.7g ˮ�������������Է�������Ϊ 30������� �ϸû�����Ļ�ѧʽΪ___��
���𰸡�4P + 5O2![]() 2P2O5 �����غ㶨�� C2H6
2P2O5 �����غ㶨�� C2H6
��������
��1��Aʵ���к����ڿ�����ȼ���������������ף���Ӧ�Ļ�ѧ����ʽΪ��4P + 5O2![]() 2P2O5��
2P2O5��
��2�����������غ㶨�ɿ�֪����ѧ�仯��Ԫ�ص��������B ʵ��õ�ˮ������Ԫ�غ���Ԫ����ɵĽ��ۣ����������������غ㶨�ɣ�
��3�������⣬��Ӧ�� CO2�� H2O���ɣ����������غ㶨�ɿ�֪���л���һ������C��H����Ԫ�أ�CO2��CԪ�ص�����=![]() ��H2O��HԪ�ص�����=
��H2O��HԪ�ص�����=![]() ��1.2g+0.3g��1.5g��˵������Ԫ����C��H��ԭ�Ӹ�����Ϊ
��1.2g+0.3g��1.5g��˵������Ԫ����C��H��ԭ�Ӹ�����Ϊ![]() �������������Է�������Ϊ30������ƶϸ����ʵĻ�ѧʽΪC2H6��
�������������Է�������Ϊ30������ƶϸ����ʵĻ�ѧʽΪC2H6��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�