题目内容
如图所示是氢氧化钙的部分性质实验,回答有关问题:
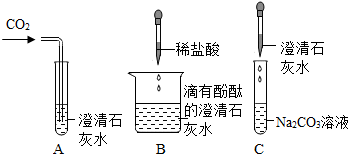
(1)C中的实验现象是 .
(2)B中发生反应的化学方程式为 .
(3)将这三个实验后的所有物质到如同一个洁净的烧杯中,静置,观察到上层溶液为无色,底部有白色沉淀.取少量上层溶液与足量稀盐酸混合,无明显现象,综合分析可知:上层溶液中一定含有的溶质是酚酞和 .

(1)C中的实验现象是
(2)B中发生反应的化学方程式为
(3)将这三个实验后的所有物质到如同一个洁净的烧杯中,静置,观察到上层溶液为无色,底部有白色沉淀.取少量上层溶液与足量稀盐酸混合,无明显现象,综合分析可知:上层溶液中一定含有的溶质是酚酞和
考点:碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的碱 碱的通性
分析:(1)C中发生的反应是氢氧化钙与碳酸钠发生复分解反应,有沉淀碳酸钙生成;
(2)稀盐酸与氢氧化钙发生反应生成氯化钙和水,据此书写化学反应方程式,注意配平;
(3)根据甲、乙、丙反应后的溶液以及三种溶液可能发生的反应进行分析.
(2)稀盐酸与氢氧化钙发生反应生成氯化钙和水,据此书写化学反应方程式,注意配平;
(3)根据甲、乙、丙反应后的溶液以及三种溶液可能发生的反应进行分析.
解答:解:(1)C中的反应是:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.CaCO3是一种白色沉淀.
故答案是:出现白色沉淀;
(2)反应物是氢氧化钙和盐酸,生成物是氯化钙和水,根据化学式的书写原则写出方程式.
故答案为:Ca(OH)2+2HCl=CaCl2+2H2O;
(3)上层溶液为无色,说明溶液中无碱性物质,溶液显酸性或中性;底部有白色沉淀.可知是反应生成的碳酸钙沉淀,说明溶液中无酸性、碱性物质,故溶液中无氢氧化钙、盐酸、碳酸钠;综合分析可知:上层溶液中一定含有的溶质是酚酞和生成的氯化钠;可能含有的溶质是氯化钙.
故答案为:NaCl、CaCl2.
故答案是:出现白色沉淀;
(2)反应物是氢氧化钙和盐酸,生成物是氯化钙和水,根据化学式的书写原则写出方程式.
故答案为:Ca(OH)2+2HCl=CaCl2+2H2O;
(3)上层溶液为无色,说明溶液中无碱性物质,溶液显酸性或中性;底部有白色沉淀.可知是反应生成的碳酸钙沉淀,说明溶液中无酸性、碱性物质,故溶液中无氢氧化钙、盐酸、碳酸钠;综合分析可知:上层溶液中一定含有的溶质是酚酞和生成的氯化钠;可能含有的溶质是氯化钙.
故答案为:NaCl、CaCl2.
点评:本题主要研究了由于反应物的量不同导致的生成物就不会相同的具体反应,综合性较强.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
食品安全关系着千家万户和每个人的身体健康,食用下列食物会影响人体健康的是( )
| A、用小苏打发酵粉焙制的糕点 |
| B、用甲醛溶液浸泡的水产品 |
| C、用增铁酱油调味的煮熟面条 |
| D、用加钙氯化钠腌制的 鱼肉 |