题目内容
下列是某些盐与酸反应的化学方程式,分析后回答问题.
①AgNO3+HCl=AgCl↓+HNO3
②Ag2CO3+2HNO3=2AgNO3+H2CO3 (H2O+CO2↑)
③Na2CO3+2HNO3=2NaNO3+H2O+CO2↑
(1)由反应①可知氯化银 (填写“能”或“不能”)和稀硝酸反应.
(2)由上述三个反应可知,盐和酸反应生成新盐和新酸,但是却不能用硝酸银和碳酸反应制取硝酸,原因是 .
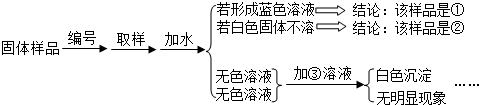
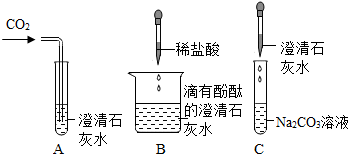
(3)若要验证一种无色溶液中含有碳酸钠、氯化钠两种溶质,就可向该溶液中加入过量的稀硝酸,有 产生则说明含有碳酸钠,再加入硝酸银溶液,有白色沉淀出现则含有氯化钠.其中加入过量的稀硝酸其目的是 .
①AgNO3+HCl=AgCl↓+HNO3
②Ag2CO3+2HNO3=2AgNO3+H2CO3 (H2O+CO2↑)
③Na2CO3+2HNO3=2NaNO3+H2O+CO2↑
(1)由反应①可知氯化银
(2)由上述三个反应可知,盐和酸反应生成新盐和新酸,但是却不能用硝酸银和碳酸反应制取硝酸,原因是
(3)若要验证一种无色溶液中含有碳酸钠、氯化钠两种溶质,就可向该溶液中加入过量的稀硝酸,有
考点:盐的化学性质
专题:常见的盐 化学肥料
分析:(1)由化学方程式,进行分析;
(2)考虑强酸制弱酸的原理;(3)考虑碳酸根与酸反应生成二氧化碳.
(2)考虑强酸制弱酸的原理;(3)考虑碳酸根与酸反应生成二氧化碳.
解答:解:
(1)由反应①AgNO3+HCl=AgCl↓+HNO3可知,氯化银不能和稀硝酸反应,如果能反应,则不能共存.
(2)至于强酸制弱酸的原理,你可以想想,假设硝酸银和碳酸反应生成碳酸银和硝酸,而生成碳酸银和硝酸,两者不共存,会继续反应生成碳酸和硝酸银.故弱酸不能制强酸.
(3)若要验证一种无色溶液中含有碳酸钠、氯化钠两种溶质,就可向该溶液中加入过量的稀硝酸,因为碳酸根与酸反应生成二氧化碳,则如果有使澄清石灰水变浑浊的气体产生则说明含有碳酸钠.再加入硝酸银溶液,因为氯离子与银离子生成氯化银,故如果有白色沉淀出现则含有氯化钠.其中加入过量的稀硝酸其目的是使碳酸钠充分反应,防止碳酸根与银离子生成碳酸银沉淀,干扰实验结论.
故答案为:
(1)不能.
(2)弱酸不能制强酸.
(3)使澄清石灰水变浑浊的气体;使碳酸钠充分反应.
(1)由反应①AgNO3+HCl=AgCl↓+HNO3可知,氯化银不能和稀硝酸反应,如果能反应,则不能共存.
(2)至于强酸制弱酸的原理,你可以想想,假设硝酸银和碳酸反应生成碳酸银和硝酸,而生成碳酸银和硝酸,两者不共存,会继续反应生成碳酸和硝酸银.故弱酸不能制强酸.
(3)若要验证一种无色溶液中含有碳酸钠、氯化钠两种溶质,就可向该溶液中加入过量的稀硝酸,因为碳酸根与酸反应生成二氧化碳,则如果有使澄清石灰水变浑浊的气体产生则说明含有碳酸钠.再加入硝酸银溶液,因为氯离子与银离子生成氯化银,故如果有白色沉淀出现则含有氯化钠.其中加入过量的稀硝酸其目的是使碳酸钠充分反应,防止碳酸根与银离子生成碳酸银沉淀,干扰实验结论.
故答案为:
(1)不能.
(2)弱酸不能制强酸.
(3)使澄清石灰水变浑浊的气体;使碳酸钠充分反应.
点评:本题主要考查了眼的化学性质,注意“碳酸根与酸反应生成二氧化碳”的利用.

练习册系列答案
相关题目
在配制溶液过程中,下列操作图示错误的是( )
A、 |
B、 |
C、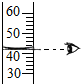 |
D、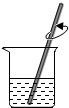 |