��Ŀ����
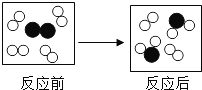
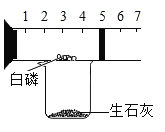
����Ŀ������̽��һ��������A�ijɷ֣���֪���п��ܺ���NH4Cl��CuCl2��FeCl3��MgCl2��BaCO3���������е����ֻ���֡���ͼ��ʾ����ʵ�飮���ֵ�������ͼ������(����������п��ܷ����ķ�Ӧ��ǡ����ȫ����)���Ը���ʵ����̺ͷ��������������жϣ���д���¿հף�

������C�Ļ�ѧʽΪ__________������F��ˮ��Һ��__________(�����ԡ����ԡ�����֮һ)
������B��һ�����е����ʵĻ�ѧʽΪ_______________
����ҺE�У�һ�����ڵ����ʵ���������__________________(д���ӷ���)
����ҺH�У������Ժ���____________������(��д����)
��д�����ɳ���G�Ļ�ѧ����ʽ______________
���ڻ����A������������ʵ��п϶������ڵ�������___(д��ѧʽ)�����������___
���𰸡�NH3 ���� Cu(OH)2 NH4+��Cu2+ 5 BaCO3 +H2 SO4 =BaSO4��+H2O+CO2�� FeCl3 �Ȼ�������Һ���Ի�ɫ������ҺE����ɫ
��������
笠����Ӻ��������Ʒ�Ӧ�����ɰ��������������ӻ���þ���ӡ�ͭ���ӡ������ӷ�Ӧ����������þ��������ͭ���������������������̼�ᱵ��Ӧ���������ᱵ������ˮ�Ͷ�����̼�������Ӻ������ӷ�Ӧ�����ɰ�ɫ���Ȼ������������Ի����A���������Ʒ�Ӧ����������ģ�ֻ���������ƺ��Ȼ�立�Ӧ���ɰ���������ɫ����A��һ�������Ȼ�泥��������ƺ��Ȼ�立�Ӧ�����Ȼ��ơ�ˮ�Ͱ���������C�ǰ�����������ˮ��Һ�Լ��ԣ���ɫ��ҺD�к����Ȼ��ƣ������A�м������ᣬ��õ���ɫ��Һ������A��һ�������Ȼ�ͭ����������ɫ����Ͱ�ɫ����������A��һ������̼�ᱵ��̼�ᱵ�����ᷴӦ�������ᱵ������ˮ�Ͷ�����̼��FeCl3��Һ�Ի�ɫ����ҺE����ɫ����һ������FeCl3�����Ͽ�֪�������A��һ����NH4Cl��CuCl2��BaCO3��һ��û��FeCl3��������MgCl2��
��1������C�Ļ�ѧʽΪNH3 ������F�Ƕ�����̼��ˮ��Һ�����ԣ�
��2������B��һ�����е����ʵĻ�ѧʽΪCu(OH)2��
��3����ҺE�У�һ�����ڵ����ʵ��������ǣ�NH4+��Cu2+ ��
��4����ҺH�У������Ժ�������ͭ������þ�������ơ����ᡢ������5�����ʣ�
��5�����ɳ���G �ķ�Ӧ��̼�ᱵ�����ᷴӦ�������ᱵ������ˮ�Ͷ�����̼����ѧ����ʽΪ��BaCO3 +H2 SO4 =BaSO4��+H2O+CO2����
��6���ڻ����A������������ʵ��п϶������ڵ�������FeCl3�������ǣ��Ȼ�������Һ���Ի�ɫ������ҺE����ɫ��

 ��������ϵ�д�
��������ϵ�д� ��ӡ�Ļ���ʱ����ϵ�д�
��ӡ�Ļ���ʱ����ϵ�д�