题目内容
【题目】(1)写出下列物质的颜色
二氧化锰 __________; 氯酸钾 ___________; 氧化铜 _________;
(2)写出下列物质的化学式
水 ________ 干冰 _________ 五氧化二磷 _______ 氮气________
(3)写出下列反应的文字表达式
①铁在氧气燃烧 _________________________________;
②蜡烛燃烧 _____________________________________;
③碳酸氢铵受热分解 ___________________________________;
④将二氧化碳通入澄清石灰水中 ____________________________________;以上反应中,既是化合反应,又是氧化反应的是 _____________(填序号)。
【答案】黑色白色黑色H2OCO2P2O5N2铁+氧气![]() 四氧化三铁蜡烛+氧气
四氧化三铁蜡烛+氧气![]() 水+二氧化碳碳酸氢铵
水+二氧化碳碳酸氢铵![]() 氨气+水+二氧化碳二氧化碳+澄清石灰水→碳酸钙+水①
氨气+水+二氧化碳二氧化碳+澄清石灰水→碳酸钙+水①
【解析】
(1)二氧化锰是黑色固体;氯酸钾是白色固体;氧化铜是黑色固体;
(2)水的化学式是H2O;干冰是固态的二氧化碳,化学式为CO2;五氧化二磷化学式为P2O5;氮气化学式为N2
(3)
①铁在氧气中燃烧生成四氧化三铁,其文字表达式为:铁+氧气![]() 四氧化三铁;
四氧化三铁;
②蜡烛燃烧生成水和二氧化碳,其文字表达式为:蜡烛+氧气![]() 水+二氧化碳;
水+二氧化碳;
③碳酸氢铵受热后分解为氨气、水和二氧化碳,其文字表达式为:碳酸氢铵![]() 氨气+水+二氧化碳;
氨气+水+二氧化碳;
④二氧化碳通入澄清石灰水中,会和氢氧化钙反应生成碳酸钙和水,其文字表达式为:二氧化碳+澄清石灰水![]() 碳酸钙+水;
碳酸钙+水;
化合反应具有“多变一”的特征,氧化反应是有氧气参与的反应,故既是化合反应,又是氧化反应的是①。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
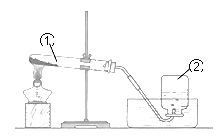
小学生10分钟应用题系列答案【题目】空气是一种宝贵的自然资源。某兴趣小组的同学在实验室欲用下图所示装置粗略测定空气中氧气的含量。
(实验回顾)
(1)写出红磷燃烧的文字表达式:____________。
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内____________减小,烧杯中水倒吸到集气瓶。若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量。
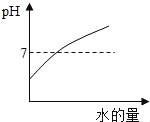
(提出问题)有实验资料表明:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测定结果与理论值误差较大。那么,能否设计一套实验装置使测定结果更为准确呢?
(查阅资料)铁生锈的原理是:铁与空气中的氧气和水蒸气等发生化学反应。饱和食盐水、活性炭会加速铁生锈。
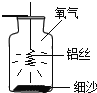
(实验改进)方案一:Ⅰ.同学们根据铁在空气中生锈的原理设计如图的实验装置,再次测定空气中氧气含量。

Ⅱ.测得实验数据如下表:
测量项目 | 实验前 | 实验后 | |
烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的体积 | |
体积/ml | 80.0 | 54.5 | 126.0 |
(交流表达)
(3)从实验原理角度分析,改进后的实验结果比前者准确度更高的原因是:①_______________;②____________。
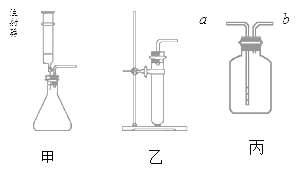
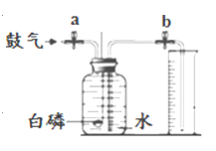
方案二:同学们又设计了下图所示的实验装置,实验步骤如下(装置气密性良好,部分操作已略去):
Ⅰ.打开止水夹a和b,向集气瓶中缓慢鼓入一定量空气,至白磷与空气接触,测得进入量筒中水的体积为V1;II.关闭a和b强光照射引燃白磷;III.白磷熄灭并冷却至室温,打开止水夹b测得量筒中水的体积变为V2;IV.计算空气中氧气的体积分数。步骤IV中,求得氧气的体积分数等于___。
【题目】(实验探究)
![]() 问题情景
问题情景
学习化学的重要途径是科学探究.安全地进行实验是你实验获得成功的重要保证!实验中涉及一系列的基本操作:取用固体药品、取用液体药品、量取液体、给物质加热、仪器洗涤等.学会规范的基本操作是实验成功的前提.
![]() 分析与结论
分析与结论
取用方法 | 原因分析 | 获得结论 | ||
粉状固体 | _________ | _________ | _________ | |
块状固体 | _________ | _________ | ||
液体药品 | 倾倒 | _________ | _________ | |
量取 | ||||