题目内容
将20gNaCl和CaCl2的混合物,溶于90g水中,向混合后的溶液中加入100g10.6%的Na2CO3溶液,恰好完全反应,求
(1)产生的沉淀质量?
(2)反应后溶液中溶质的质量分数?
(1)产生的沉淀质量?
(2)反应后溶液中溶质的质量分数?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据CaCl2和NaCl的混合物形成的溶液中,加入Na2CO3溶液,CaCl2能与Na2CO3溶液反应生成碳酸钙沉淀和氯化钠,据此由碳酸钠的质量求出碳酸钙的质量;
(2)反应后所得滤液为氯化钠溶液,包括原混合物中的氯化钠和反应生成的氯化钠,反应后所得溶液的质量是用所有物质的质量总和-生成沉淀的质量.由溶质质量分数的计算公式计算出溶质的溶质质量分数即可.
(2)反应后所得滤液为氯化钠溶液,包括原混合物中的氯化钠和反应生成的氯化钠,反应后所得溶液的质量是用所有物质的质量总和-生成沉淀的质量.由溶质质量分数的计算公式计算出溶质的溶质质量分数即可.
解答:解:设设混合物中CaCl2的质量为x,生成的NaCl的质量为y,产生的沉淀质量为z
CaCl2 +Na2CO3 =2NaCl+CaCO3↓
111 106 117 100
x 100g×10.6% y z
=
=
=
x=11.1g,y=11.7g,z=10g
反应后滤液中氯化钠的质量为:20g-11.1g+11.7g=20.6g,
反应后滤液质量为:20g+90g+100g-10g=200g
反应后溶液中溶质的质量分数:
×100%=10.3%.
答:(1)产生的沉淀质量10g;
(2)反应后溶液中溶质的质量分数为10.3%.
CaCl2 +Na2CO3 =2NaCl+CaCO3↓
111 106 117 100
x 100g×10.6% y z
| 111 |
| x |
| 106 |
| 100g×10.6% |
| 117 |
| y |
| 100 |
| z |
x=11.1g,y=11.7g,z=10g
反应后滤液中氯化钠的质量为:20g-11.1g+11.7g=20.6g,
反应后滤液质量为:20g+90g+100g-10g=200g
反应后溶液中溶质的质量分数:
| 20.6g |
| 200g |
答:(1)产生的沉淀质量10g;
(2)反应后溶液中溶质的质量分数为10.3%.
点评:本题难度较大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,反应后所得溶液的质量的方法一般是用所加的所有物质的质量总和-生成沉淀的质量(或生成气体的质量).

练习册系列答案
相关题目
下列有关金属材料的描述正确的是( )
| A、铁、铝、铜都是银白色金属 |
| B、纯铝片比硬铜片的硬度大 |
| C、生铁和铜都是铁的单质 |
| D、回收利用废旧电池中的铅、汞等可减少对环境的污染 |
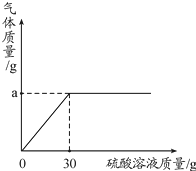 草木灰是农家肥料,它的主要成分是碳酸钾,还有硫酸钾、氯化钾等.化学兴趣小组为测定某草木灰样品中的有效成分,取100g草木灰于烧杯中,不断滴入稀硫酸溶液,当滴入30g稀硫酸时,不再有气泡产生,此时烧杯中的残余混合物质量为127.8g.碳酸钾与硫酸反应的化学方程式为K2CO3+H2SO4═K2SO4+CO2↑+H2O (假设草木灰的其他成分不含钾元素、不与酸反应)
草木灰是农家肥料,它的主要成分是碳酸钾,还有硫酸钾、氯化钾等.化学兴趣小组为测定某草木灰样品中的有效成分,取100g草木灰于烧杯中,不断滴入稀硫酸溶液,当滴入30g稀硫酸时,不再有气泡产生,此时烧杯中的残余混合物质量为127.8g.碳酸钾与硫酸反应的化学方程式为K2CO3+H2SO4═K2SO4+CO2↑+H2O (假设草木灰的其他成分不含钾元素、不与酸反应)