题目内容
【题目】金属在生产、生活中有广泛的用途。
(1)铝块能制成用于包装的铝箔,是由于铝具有________。工业上常用电解氧化铝的方法制铝,电解中需加入助熔剂——冰晶石(Na3AlF6),其中氟元素的化合价为________。
(2)汽车车体表面喷漆不仅美观,而且可有效防止钢铁与________接触而生锈。
(3)铁是世界上年产量最高的金属。用一氧化碳还原氧化铁的化学方程式为__________。
(4)将一定量铁粉加入到硫酸锌和硫酸铜的混合溶液中,充分反应后过滤。滤液中的溶质一定有________,证明滤渣中成分的实验方案是_________,可能的现象与结论是________。
【答案】延展性 -1 氧气和水(填符号也可) 硫酸锌、硫酸亚铁 取少量滤渣加入稀盐酸 若产生气泡,成分是铁和铜 若无气泡,成分是铜(答一种即可)
【解析】
(1)铝能制成用于包装的铝箔,是由于铝具有良好的延展性;设氟元素的化合价为x,在Na3AlF6中,钠元素的化合价是+1,铝元素的化合价是+3,则有:(+1)×3+(+3)×1+x×6=0,x=-1;
(2)铁在与氧气和水蒸气同时接触时会生锈,在车体表面喷漆可以防止铁与氧气、水蒸气接触而生锈;
(3)一氧化碳还原氧化铁的化学方程式为:3CO+Fe2O3![]() 2Fe+3CO2;
2Fe+3CO2;
(4)由于在金属活动顺序表中,铁在铜的前面,在锌的后面,所以向硫酸铜和硫酸锌的混合溶液中加入一定量的铁粉,铁可以硫酸铜溶液反应生成铜和硫酸亚铁,不能和硫酸锌发生反应;充分反应后过滤,得到滤渣和滤液,如果铁粉过量,则滤渣中含有铁粉和铜粉,如果铁粉恰好完全反应,则滤渣中只有铜,所以滤渣中一定有铜;无论铁粉是否过量,滤液中都一定有反应后生成的硫酸亚铁和不和铁发生反应的硫酸锌;证明滤渣中成分的实验方案是:取少量滤渣,加入稀盐酸,若产生气泡则滤渣成分为铁和铜;若无明显现象则滤渣成分为铜。

【题目】FeCl3(氯化铁)溶液也能对过氧化氢的分解能起催化作用,某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响。
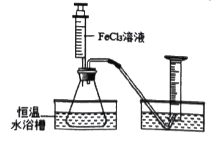
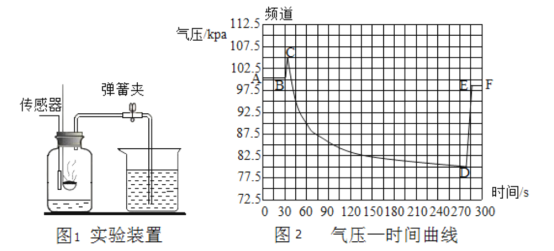
Ⅰ.分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的FeCl3溶液,通过观察______,就可以粗略判断,得到实验结果,为进一步判断上述试验结论的准确性,运用图示装置,小刚同学进行了如下实验方案设计进行定量研究。
Ⅱ.[方案一]在不同过氧化氢浓度下,测定收集相同体积气体所需的时间。
[方案二]在不同过氧化氢浓度下,测定_________。
方案二的实验测量结果:
物理量 序号 | H2O2溶液的浓度和体积 | 2% FeCl3溶液的 体积(mL) | 反应的时间 ( min) | 生成O2的体积 (mL) |
1 | 30%,10mL | x | 5 | V1 |
2 | 10%,10mL | 3 | y | V2 |
(1)表中x=_________,y=_______。
(2)通过测量,若V1_______V2(填“>”、“=”或“<”) 得出的实验结论为_____。