题目内容
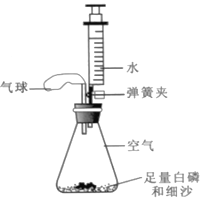
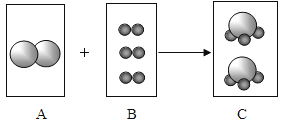
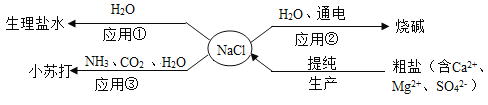
【题目】化学课上,同学们利用下列分组实验来探究碱的化学性质:
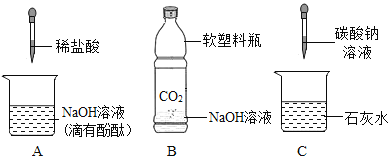
(1)做B组实验的同学看到了明显的现象是_____。
(2)实验结束,同学们将废液(废渣除外)倒入同一只废液缸中,最后发现废液呈无色。
[提出问题]废液中含有什么物质?
[猜想与假设]通过分析上述实验,同学们猜想:废液中一定含有_____。废液中的溶质(忽略酚酞)的成分引发了同学们的热烈讨论,下面是两位同学的发言:
小龙:氯化钠
小江:氯化钠、氯化氢
还可能是_____或_____;
[实验验证]小美同学对可能含有的溶质进行确定,取一定量的废液,向其中滴加几滴碳酸钠溶液,只看到_____的现象,小美确定小江猜想正确;
[反思与评价]小美同学由实验得出的结论_____(填写“正确”或“不正确”)。
[结论与应用]在得知小江同学猜想错误后,老师要求同学们从废液中回收氯化钠固体(利用已有的一种化学药品),你的具体操作方法是_____。
【答案】塑料瓶变瘪 氯化钠 氯化钠和氯化钙 氯化钠、氯化氢和氯化钙 有气泡产生 不正确 先滴加适量的碳酸钠溶液去除氯化氢、氯化钙,然后过滤,对滤液蒸发结晶,对氯化钠固体洗涤干燥,即可得到精盐氯化钠
【解析】
(1)因为二氧化碳能与氢氧化钠发生化学反应生成碳酸钠,瓶内气体减少,气压降低,在大气压的作用下,塑料瓶子变瘪;故填;塑料瓶变瘪;
[猜想与假设]废液中一定有酚酞和生成的氯化钠,因为废液是无色的,所以废液中一定没
有碳酸钠、氢氧化钙、氢氧化钠,可能有氯化氢、氯化钙;故填;氯化钠;
根据实验现象分析可知,废液中一定有氯化钠,可能还存在氯化氢或氯化钙,因此废液中.
的溶质有四种情况:只有氯化钠;氯化钠和氯化氢;氯化钠和氯化钙;氯化钠、氯化氢和氯化钙;故填:氯化钠和氯化钙;氯化钠、氯化氢和氯化钙;
[实验验证]若小江猜想正确,也就是溶质为氯化钠和氯化氢,则加入碳酸钠溶液后,会生
成二氧化碳气体,故填:有气泡产生;
[反思与评价]若废液中含有氯化钠、氯化氢和氯化钙,加入碳酸钠也会生成气体;应该加
入过量的碳酸钠溶液,只有气泡产生,则废液中只含有氯化钠、氯化氢;若开始生成气体,
后又有白色沉淀生成,则其中还含有氯化钙;故填:不正确;
[结论与应用]在得知小江同学猜想错误后,那么溶液的组成,只可能是氯化钠;氯化钠、氯化钙;氯化钠、氯化钙、氯化氢,可先先滴加适量的碳酸钠溶液去除氯化氢、氯化钙,然后过滤,对滤液蒸发结晶,即可得到氯化钠,故填:先滴加适量的碳酸钠溶液去除氯化氢、氯化钙,然后过滤,对滤液蒸发结晶,对氯化钠固体洗涤干燥,即可得到精盐氯化钠 。

 名校课堂系列答案
名校课堂系列答案【题目】某同学向一定质量的石灰石中加入7.3%的稀盐酸来制取二氧化碳,测得反应过程中溶液的pH与加入的稀盐酸的关系如右图所示。

(1)该同学能收集到的二氧化碳的质量多少?(写出计算过程)
(2)该同学把制取气体后的废液过滤,向滤液中加入10.6%的Na2CO3溶液,测得加入的Na2CO3溶液与产生的沉淀数据如下:
Na2CO3溶液质量/g | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
沉淀质量/g | 0 | 1 | n | 3 | 4 | 5 | m |
则m= 。加入10gNa2CO3溶液时发生反应的化学方程式是 。
请在右图中画出向废液中加入Na2CO3溶液时加入的Na2CO3溶液与产生的沉淀的曲线。

【题目】在学习金属的化学性质时,老师在课堂上给学生们演示了如图实验:
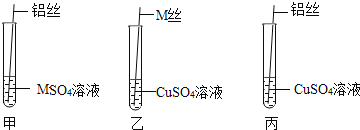
(给出资料)M是一种金属,![]() 溶液是无色液体。
溶液是无色液体。
(实验目的)探究M与铜、铝的活动性顺序。
(猜想与假设)
猜想Ⅰ:![]() ;
;
猜想Ⅱ:![]() ;
;
猜想Ⅲ:_____。
(进行实验)
第一步:老师取出M丝、铜丝、铝丝用砂纸进行打磨,目的是_____。
第二步:老师按照如图进行实验操作,要求同学们填写如下表格:
实验操作 | 实验想象 | 实验结论 |
铝丝插入装有 | 铝丝表面出现一层黑色物质 | _____ |
M丝插入装有 | M丝表面出现一层红色物质,溶液的颜色_____。 | M>Cu |
铝丝插入装有 | M丝表面出现一层红色物质,颜色由蓝色变为无色 | Al>Cu |
第三步:根据表格,可判断猜想_____正确。
(交流表达)
老师要求同学们写出试管丙中反应的化学方程式_____。然后经同学们讨论后大家认为该实验可以优化,去掉试管_____![]() 填试管编号
填试管编号![]() 中的实验,也可以得出正确的结论。
中的实验,也可以得出正确的结论。
(评价与反思)
实验结束后,同学对实验过程进行了如下反思:如果M能够和稀酸溶液反应,探究金属![]() 铜、铝活动性顺序时,除了上述实验中已经用到的方法外,还可以根据_____进行判断
铜、铝活动性顺序时,除了上述实验中已经用到的方法外,还可以根据_____进行判断![]() 任写一种
任写一种![]() 。
。
【题目】戴口罩、勤洗手,给自己居住、生活的环境消消毒,都是预防新型冠状病毒感染的有效方法。其中“84”消毒液能用于日常生活的消毒灭菌。某化学兴趣小组对一瓶 敞口放置的“84”消毒液成分产生兴趣,在老师的指导下进行如下探究:
(提出问题)该敞口久置的“84”消毒液中含有哪些溶质?
(查阅资料)(1)“84”消毒液主要成分是次氯酸钠(NaClO)和氯化钠,NaClO 为有效成分,有腐蚀性,并易与空气中 CO2 反应(2NaClO+CO2+H2O=2HClO+Na2CO3)。
(2)次氯酸(HClO)溶液和次氯酸钠(NaClO)溶液都具有漂白、杀菌、消毒功效。
(3)HClO 不稳定,受热或光照易分解。
(提出猜想)I.“84”消毒液没有变质
II.____________
III.“84”消毒液完全变质
(设计方案)为验证猜想,设计如下方案:
实验操作 | 实验现象 | 结论 |
(1)另取该消毒液少量于试管中,滴加足量 BaCl2 溶液,振荡 | 产生白色沉淀 | 猜想________不成立,反应的化学方程式是____________。 |
(2)向盛有有色布条的烧杯中滴加该消毒液适量,放置一段时间 | 有色布条_________。(填“褪色”或“不褪色” | 猜想 II 不成立,猜想 III 成立 |
(得出结论)综上所述,该敞口放置的“84”消毒液中溶质一定有____________________。
(拓展延伸)
(1)次氯酸钠与盐酸反应会生成有毒的黄绿色气体单质,该气体单质是____________,因此,“84”消毒液____________________(填“能”或“不能”)与洁厕灵(主要成分为盐酸)混合使用。
(2)欲用 40%的 NaClO 溶液稀释配制 25%的溶液 400g,需要加水__________g。