题目内容
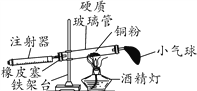
【题目】如下图是测定空气中氧气含量的实验装置图。实验如下:用注射器抽取30 mL空气(活塞拉至30mL刻度处),硬质玻璃管中空气的体积为50 mL;在硬质玻璃管中放入过量铜粉,在右侧导管口套上瘪的气球;点燃酒精灯,反复推拉注射器和挤压气球,待充分反应后,冷却至室温;将气球中气体全部挤入硬质玻璃管,注射器中气体的体积为14 mL。
(1)写出铜粉与氧气反应的化学方程式:__________________。
(2)实验时,铜粉过量的目的是________;________(填“能”或“不能”)用木炭代替铜粉进行相同实验。
(3)实验测得空气中氧气的含量为________。
【答案】 2Cu+O2![]() 2CuO 使硬质玻璃管中的氧气完全反应 不能 20%(或
2CuO 使硬质玻璃管中的氧气完全反应 不能 20%(或![]() )
)
【解析】本题考查了空气中氧气的含量的测定。理解测定原理是解题的关键。
(1)铜粉与氧气加热时反应生成氧化铜;发生反应的化学方程式为2Cu+O2![]() 2CuO;
2CuO;
(2)实验时,为了完全除去空气中的氧气,铜粉必须是过量的,使硬质玻璃管中的氧气完全反应,否则得出的结果不准确;铜粉与氧气反应生成固体氧化铜,而木条与氧气反应生成二氧化碳气体,瓶内气压基本不变,无法测量氧气的含量,不能用木炭代替铜粉进行相同实验;
(3)原装置内气体为30mL+50mL=80ml;待充分反应后,冷却至室温;将气球中气体全部挤入硬质玻璃管,注射器中气体的体积为14mL,则反应消耗氧气的体积为30mL-14mL=16mL;实验测得空气中氧气的含量为: ![]() ×100%=20%(或
×100%=20%(或![]() )。
)。

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目