题目内容
【题目】(9分)某化学兴趣小组的同学对空气中氧气的含量进行探究。
【提出问题】空气中氧气的含量是多少?
【查阅资料】①红磷和白磷都能在空气中燃烧,都生成五氧化二磷,但红磷的着火点(可燃物燃烧所需的最低温度)为240℃,白磷的着火点为40℃。
②氧化钙能与反应生成氢氧化钙,同时放出大量的热,能煮熟鸡蛋。
③生石灰的主要成分是氧化钙。
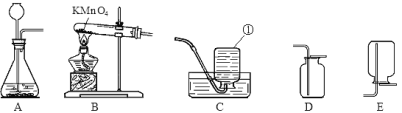
【设计方案】兴趣小组的同学将一个具有刻度和可滑动活塞的玻璃管(其中有空气和白磷)放在装有生石灰的烧杯的上方(如图所示),用此装置进行实验,请你一同参与。
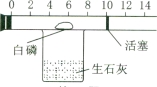
【进行实验】①检查图中玻璃管的气密性。其操作步骤、现象和结论是
②按图示装好药品后的操作是 该操作的作用是
【记录现象】实验过程中观察到的现象是
【实验结论】
【实验反思】本实验是对教材实验稍作改进而设计的,其主要优点是
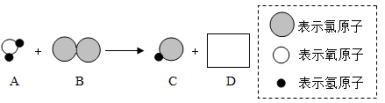
【拓展与应用】已知, 据此反应能否用镁代替磷测定空气中氧气的体积含量?
![]()
由此你对氮气的化学性质有何新的认识
【答案】【进行实验】①用热毛巾捂住玻璃管,活塞右移,把热毛巾取走,活塞又回到原刻度(合理均对)
②向烧杯中加入适量的水 利用水和生石灰反应放出的热量,引燃白磷。
【记录现象】①白磷燃烧,产生大量白烟 ②先向右移,后向左移 ③8
【实验结论】氧气约占空气总体积的1/5
【实验反思】实验操作均在密闭容器中进行,减小测量误差
【拓展与应用】不能 氮气的化学性质不活泼是相对的,在一定条件下,氮气也能跟其他物质发生化学反应
【解析】
试题分析:【进行实验】①该装置的气密性良好即装置不漏气,那么可用热毛巾捂住玻璃管,活塞右移,把热毛巾取走,活塞又回到原刻度,说明装置的气密性良好;
②测定空气成分的原理是物质与氧气反应导致压强变小。由于白磷燃烧需要达到一定的温度,根据资料,白磷燃烧所需的热量由生石灰与水反应提供,故接下来的步骤是向烧杯中加入适量的水;
【记录现象】白磷燃烧,产生大量的白烟,同时会放出大量的热,故开始时活塞会向右边移动,当白磷熄灭,装置冷却后,由于消耗了氧气,导致装置内的压强变小,故活塞又会向左移动;由于氧气约占空气总体积的1/5,据图可知空气的总体积为10ml,故活塞最终停在8ml位置;
【实验结论】该实验可得出氧气约占空气总体积的1/5;
【实验反思】由于实验操作均在密闭容器中进行,可减小测量误差;
【拓展与应用】由于镁既能与氧气还能与空气中氮气反应,会导致装置中的压强变化很大,故不能用镁代替;由此可知氮气也能与气体的物质发生化学反应。

 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案