题目内容
1、海水是一种化学成分复杂的混合物,包括水、溶解于水中的多种化学元素和气体.在海水中迄今已发现的化学元素达80多种.含量较高的元素除组成水的氢、氧元素外,还有氯、钠、镁、硫、钙、钾、溴、碳、锶、硼、氟等.
(1)以海水及其产品为原料可以生产许多化工产品,如氯化钠、氢气、氢氧化钠、氯气、钠、镁、食用加碘盐等.
①请根据你学过的化学知识,按照纯净物、单质、混合物、化合物,将海水、氢气、氯化钠、氯气、氢氧化钠、钠、镁、食用加碘盐进行分类.(要求用框图的形式表示,层次分明)
②在氯化钠、氢气、镁三种物质中,由分子构成的是
(2)自然界中的溴元素绝大多数存在于海洋中,其元素符号为Br,根据中文名称猜测溴应属于
(3)锶是一种重要的金属元素,其原子结构示意图和在元素周期表中显示的信息见下图,请回答有关问题: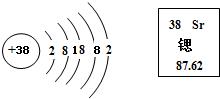
①锶原子核外的电子层数为
②锶元素的原子序数为
(4)海水也是未来人类生活用水的重要来源.小明同学从水产市场带回一瓶浑浊的海水,准备与同学们一起对其进行净化.请你参入他们的实验并回答有关问题.
①他们在向水中加入明矾,搅拌静置后进行过滤,加入明矾的目的是
②下列对过滤过程及结果描述正确的是(ABC )(填编号);
A.此过程发生的是物理变化
B.过滤是利用颗粒大小不同将混合物分离
C.过滤之后得到的“水”仍是咸的
D.过滤之后得到的“水”可以饮用
③证明过滤之后得到的“水”中仍含有杂质的方法是
④小明想把海水制成蒸馏水,他应该进行的操作是
一般不用蒸馏水作为饮用水的理由是
(5)海水是一种溶液,其中溶剂是水,溶质有多种,海水中溶质的质量分数约为3.5%,市场上销售的“海水精”是根据海水溶质的主要成分按比例混合而成,“海水精”是一种白色固体,易溶于水.若用“海水精”配制一定量的人造海水,请回答有关问题:
①配制步骤依次为
②所需要用到的主要仪器是
(1)以海水及其产品为原料可以生产许多化工产品,如氯化钠、氢气、氢氧化钠、氯气、钠、镁、食用加碘盐等.
①请根据你学过的化学知识,按照纯净物、单质、混合物、化合物,将海水、氢气、氯化钠、氯气、氢氧化钠、钠、镁、食用加碘盐进行分类.(要求用框图的形式表示,层次分明)
②在氯化钠、氢气、镁三种物质中,由分子构成的是
氢气
;由原子构成的是镁
;由离子构成的是氯化钠
.(2)自然界中的溴元素绝大多数存在于海洋中,其元素符号为Br,根据中文名称猜测溴应属于
非金属
(填“金属”或“非金属”)元素,该元素位于元素周期表右侧
(填“左侧”、“右侧”或“中部”).(3)锶是一种重要的金属元素,其原子结构示意图和在元素周期表中显示的信息见下图,请回答有关问题:

①锶原子核外的电子层数为
5
,原子核内质子数为38
;在化学反应中易失去
(填“得到”或“失去”)电子②锶元素的原子序数为
38
,其相对原子质量为87.62
;(4)海水也是未来人类生活用水的重要来源.小明同学从水产市场带回一瓶浑浊的海水,准备与同学们一起对其进行净化.请你参入他们的实验并回答有关问题.
①他们在向水中加入明矾,搅拌静置后进行过滤,加入明矾的目的是
使水中悬浮的杂质沉降
;过滤需要的主要仪器和用品有铁架台(带铁圈)、漏斗、玻璃棒、烧杯、滤纸
;②下列对过滤过程及结果描述正确的是(ABC )(填编号);
A.此过程发生的是物理变化
B.过滤是利用颗粒大小不同将混合物分离
C.过滤之后得到的“水”仍是咸的
D.过滤之后得到的“水”可以饮用
③证明过滤之后得到的“水”中仍含有杂质的方法是
滴几滴水样于玻璃片上,放在酒精灯上加热,观察现象
;④小明想把海水制成蒸馏水,他应该进行的操作是
蒸馏
,一般不用蒸馏水作为饮用水的理由是
蒸馏水中不含人体所需的多种矿物元素,长期饮用会影响健康
.(5)海水是一种溶液,其中溶剂是水,溶质有多种,海水中溶质的质量分数约为3.5%,市场上销售的“海水精”是根据海水溶质的主要成分按比例混合而成,“海水精”是一种白色固体,易溶于水.若用“海水精”配制一定量的人造海水,请回答有关问题:
①配制步骤依次为
计算、称量(量取)、溶解
;②所需要用到的主要仪器是
托盘天平、量筒、药匙、玻璃棒、胶头滴管、烧杯
.分析:(1)①根据纯净物、单质、混合物、化合物的概念分析即可;
②根据构成物质的微观粒子分析即可;
(2)根据金属与非金属的区别及金属与非金属在元素周期表中的位置分析;
(3)根据原子结构示意图中所包含的内容分析,再根据原子最外层电子的特点分析即可;
(4)①根据明矾净水的原理及过滤所用到的仪器分析即可;
②根据过滤的原理分析即可;
③根据蒸发的原理分析即可;
④根据蒸馏的原理及蒸馏水的特点分析即可;
(5)根据配制一定溶质质量分数的溶液的操作步骤及所用到的仪器分析即可.
②根据构成物质的微观粒子分析即可;
(2)根据金属与非金属的区别及金属与非金属在元素周期表中的位置分析;
(3)根据原子结构示意图中所包含的内容分析,再根据原子最外层电子的特点分析即可;
(4)①根据明矾净水的原理及过滤所用到的仪器分析即可;
②根据过滤的原理分析即可;
③根据蒸发的原理分析即可;
④根据蒸馏的原理及蒸馏水的特点分析即可;
(5)根据配制一定溶质质量分数的溶液的操作步骤及所用到的仪器分析即可.
解答:(1)①根据纯净物、单质、混合物、化合物的概念可知,海水和加碘食盐是混合物;氢气、氯气、钠和镁是单质;氯化钠和氢氧化钠是化合物;
故答案为:

②构成物质的粒子有:原子、分子、离子,氢气由氢分子构成,金属镁是由镁原子构成的,氯化钠是由钠离子和氯离子构成的,
故答案为:氢气(H2)镁(Mg)氯化钠(NaCl);
(2)根据金属和非金属中文名称的区别可知,溴为非金属元素,在元素周期表中溴位于其右侧,
故答案为:非金属、右侧;
(3)①观察锶的原子结构示意图可知,锶元素有5个电子层,核内有38个质子,因为锶元素最外层有2个电子,个数少于4个,所以在化学反应中易失去电子,
故答案为:5、38、失去;
②根据锶元素在元素周期表中所显示的信息可知,锶元素的原子序数为38,相对原子质量为87.62,
故答案为:38、87.62;
(4)①明矾净水的原理是:明矾溶于水生成胶体,胶体可以吸附悬浮的杂质;
过滤操作中需要用到的仪器有:铁架台(带铁圈)(或漏斗架)、漏斗、玻璃棒、烧杯、滤纸;
故答案为:使水中悬浮的杂质沉降 铁架台(带铁圈)(或漏斗架)、漏斗、玻璃棒、烧杯、滤纸
②过滤操作只会把不溶于水的固体滤去,而溶于水的离子或分子仍然留在滤液中,所以过滤后的溶液中仍然有氯化钠,故过滤后的水仍然是咸水;另外过滤只是把混合物分离,并未生成新的物质,所以过滤属于物理变化;过滤过程中不溶于水的固体不会透过滤纸,留在滤纸上,而溶于水的离子或小分子可以透过滤纸;
故选ABC
③加热蒸发水时,因为水分子的沸点比较低,在加热的过程中变成气态进入大气中,而可溶性的固体沸点比较高,仍然留在玻璃片上,水蒸发完后若玻璃片上有残留固体,说明水中含有其它杂质,
故答案为:滴几滴水样于玻璃片上,放在酒精灯上加热,观察现象.
④由海水制蒸馏水的常用方法是蒸馏,因为人体需要多种矿物元素,而蒸馏水是纯净物不含矿质元素,长期饮用会影响健康,
故答案为:蒸馏、蒸馏水中不含人体所需的多种矿物元素,长期饮用会影响健康;
(5)①用固体溶质配制一定溶质质量分数溶液的操作步骤是:计算、称量(量取)、溶解;
故答案为:计算、称量(量取)、溶解
②用固体溶质配制一定溶质质量分数溶液的操作过程中所用到的仪器有:托盘天平、量筒、药匙、玻璃棒、胶头滴管、烧杯;
故答案为:托盘天平、量筒、药匙、玻璃棒、胶头滴管、烧杯.
故答案为:

②构成物质的粒子有:原子、分子、离子,氢气由氢分子构成,金属镁是由镁原子构成的,氯化钠是由钠离子和氯离子构成的,
故答案为:氢气(H2)镁(Mg)氯化钠(NaCl);
(2)根据金属和非金属中文名称的区别可知,溴为非金属元素,在元素周期表中溴位于其右侧,
故答案为:非金属、右侧;
(3)①观察锶的原子结构示意图可知,锶元素有5个电子层,核内有38个质子,因为锶元素最外层有2个电子,个数少于4个,所以在化学反应中易失去电子,
故答案为:5、38、失去;
②根据锶元素在元素周期表中所显示的信息可知,锶元素的原子序数为38,相对原子质量为87.62,
故答案为:38、87.62;
(4)①明矾净水的原理是:明矾溶于水生成胶体,胶体可以吸附悬浮的杂质;
过滤操作中需要用到的仪器有:铁架台(带铁圈)(或漏斗架)、漏斗、玻璃棒、烧杯、滤纸;
故答案为:使水中悬浮的杂质沉降 铁架台(带铁圈)(或漏斗架)、漏斗、玻璃棒、烧杯、滤纸
②过滤操作只会把不溶于水的固体滤去,而溶于水的离子或分子仍然留在滤液中,所以过滤后的溶液中仍然有氯化钠,故过滤后的水仍然是咸水;另外过滤只是把混合物分离,并未生成新的物质,所以过滤属于物理变化;过滤过程中不溶于水的固体不会透过滤纸,留在滤纸上,而溶于水的离子或小分子可以透过滤纸;
故选ABC
③加热蒸发水时,因为水分子的沸点比较低,在加热的过程中变成气态进入大气中,而可溶性的固体沸点比较高,仍然留在玻璃片上,水蒸发完后若玻璃片上有残留固体,说明水中含有其它杂质,
故答案为:滴几滴水样于玻璃片上,放在酒精灯上加热,观察现象.
④由海水制蒸馏水的常用方法是蒸馏,因为人体需要多种矿物元素,而蒸馏水是纯净物不含矿质元素,长期饮用会影响健康,
故答案为:蒸馏、蒸馏水中不含人体所需的多种矿物元素,长期饮用会影响健康;
(5)①用固体溶质配制一定溶质质量分数溶液的操作步骤是:计算、称量(量取)、溶解;
故答案为:计算、称量(量取)、溶解
②用固体溶质配制一定溶质质量分数溶液的操作过程中所用到的仪器有:托盘天平、量筒、药匙、玻璃棒、胶头滴管、烧杯;
故答案为:托盘天平、量筒、药匙、玻璃棒、胶头滴管、烧杯.
点评:元素核内质子数与原子序数相等.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目

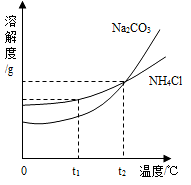
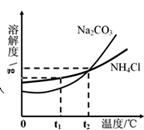
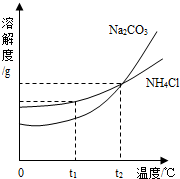 (3)我国化学科学家侯德榜创立的侯氏制碱法,就是以海水“晒盐”得到的氯化钠为原料,同时制得Na2CO3和NH4Cl产品.Na2CO3和NH4Cl的溶解度曲线如图所示.回答下列问题:
(3)我国化学科学家侯德榜创立的侯氏制碱法,就是以海水“晒盐”得到的氯化钠为原料,同时制得Na2CO3和NH4Cl产品.Na2CO3和NH4Cl的溶解度曲线如图所示.回答下列问题:
 (3)我国化学科学家侯德榜创立的侯氏制碱法,就是以海水“晒盐”得到的氯化钠为原料,同时制得Na2CO3和NH4Cl产品.Na2CO3和NH4Cl的溶解度曲线如图所示.回答下列问题:
(3)我国化学科学家侯德榜创立的侯氏制碱法,就是以海水“晒盐”得到的氯化钠为原料,同时制得Na2CO3和NH4Cl产品.Na2CO3和NH4Cl的溶解度曲线如图所示.回答下列问题: