题目内容
【题目】实验室有不纯的氯酸钾样品12.5g,把该样品与少量二氧化锰混合加热制取氧气(杂质不参加反应),反应的化学方程式为: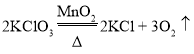 。充分反应后,固体混合物质量变化如下图所示:
。充分反应后,固体混合物质量变化如下图所示:
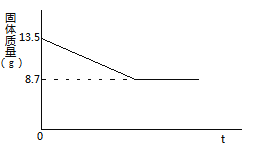
(1)生成氧气的质量为 g
(2)样品中氯酸钾的质量分数是多少?(写出计算过程)
【答案】(1)4.8 ;(2)98%
【解析】
氯酸钾分解放出氧气,所以固体混合物减少的质量就是逸出氧气的质量,然后利用化学方程式的计算,将氧气的质量带入求出氯酸钾的质量,进而得以求解样品中氯酸钾的质量分数。
(1)固体混合物减少的质量就是氧气的质量,生成氧气的质量为13.5g-8.7g=4.8g;
(2)设样品中氯酸钾的质量为![]() ,
,
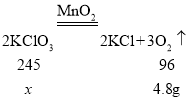
![]() ,解得
,解得![]() =12.25g
=12.25g
氯酸钾的质量分数为![]()
答:生成氧气的质量为4.8g,样品中氯酸钾的质量分数是98%。

练习册系列答案
相关题目