题目内容
相同条件下,把Al、Mg、Fe分别投入相同浓度相同体积且过量的稀H2SO4中,反应结束后三种溶液的质量仍然相等,则投入三种金属的质量关系是
- A.Mg>Al>Fe
- B.Al>Fe>Mg
- C.Fe>Mg>Al
- D.Al>Mg>Fe
D

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
| (1)钢铁是重要的金属材料,应用十分广泛 | ||||||||||
| ①生铁和钢都属于 | ||||||||||
|
[ ] | ||||||||||
| A.纯净物 B.混合物 C.金属单质 D.合金 | ||||||||||
| ②铁在空气中容易锈蚀,实际上是铁跟空气中的 共同作用的结果。 | ||||||||||
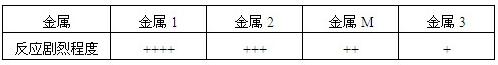
| (2)利用金属的性质回答下列问题。 在相同条件下,把金属M及另外三种金属分别加入到质量和浓度均相等的足量稀硫酸中,通过观察产生气泡的快慢,判断反应的剧烈程度,并记录如下(产生气泡的快慢用“+”表示,“+”越多,表示产生气泡越快)。 | ||||||||||
| ||||||||||
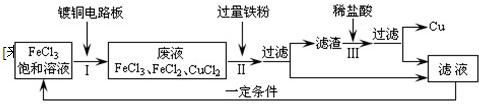
| ①如果上述金属分别是Al、Mg、Zn、Fe四种中的一种,你认为金属M最有可能是 。 氯化铁能腐蚀铜,工业上常用此原理生产印刷线路板。以下是印刷线路板的生产及废液处理过程:(其中镀铜电路板为表面上覆盖一层金属铜的线路板) | ||||||||||
 | ||||||||||
| ②步骤Ⅱ中发生了两个反应的化学方程式分别为: 2FeCl3 + Fe = 3FeCl2和 ; 步骤Ⅲ中反应的化学方程式为 ; 试写出步骤Ⅰ中氯化铁跟铜反应的化学方程式 。 |