题目内容
某化学课外活动小组用氯酸钾和二氧化锰的混合物加热制氧气,制氧气完毕后的固体混合物的主要成分是氯化钾和二氧化锰.该小组不是将反应后的固体混合物丢弃,而是对其进行分离提纯,制得纯净的氯化钾和纯净的二氧化锰.在此提纯的实验过程中,用到下列仪器次数最多的是
- A.烧杯
- B.玻璃棒
- C.蒸发皿
- D.酒精灯
B
分析:分离氯化钾和二氧化锰时,氯化钾易溶于水,而二氧化锰不溶于水,所以首先将混合物放入适量的水溶解氯化钾,然后过滤,最后再蒸发溶剂得到氯化钾.
解答:将氯化钾和二氧化锰加适量水溶解.在此过程中用玻璃棒搅拌加速溶解.然后过滤得到二氧化锰固体.在此过程中用玻璃棒转移药品.最后将氯化钾溶液加热蒸发,得氯化钾固体,在此过程中用玻璃棒搅拌,防止液体飞溅.
故选B
点评:在分离混合物时,首先考虑混合物中各组分的水溶性,若一种可溶而另一种不溶,那么可以考虑用过滤的方法分离.
分析:分离氯化钾和二氧化锰时,氯化钾易溶于水,而二氧化锰不溶于水,所以首先将混合物放入适量的水溶解氯化钾,然后过滤,最后再蒸发溶剂得到氯化钾.
解答:将氯化钾和二氧化锰加适量水溶解.在此过程中用玻璃棒搅拌加速溶解.然后过滤得到二氧化锰固体.在此过程中用玻璃棒转移药品.最后将氯化钾溶液加热蒸发,得氯化钾固体,在此过程中用玻璃棒搅拌,防止液体飞溅.
故选B
点评:在分离混合物时,首先考虑混合物中各组分的水溶性,若一种可溶而另一种不溶,那么可以考虑用过滤的方法分离.

练习册系列答案
相关题目
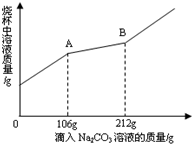 某化学课外活动小组用石灰石和稀盐酸为原料制取二氧化碳,在完成实验后,对反应后的废液进行探究.他们取过滤后的废液100g,向其中逐渐滴加溶质的质量分数为10%的Na2CO3溶液,烧杯中溶液的质量与所滴入Na2CO3溶液的质量关系如图所示:
某化学课外活动小组用石灰石和稀盐酸为原料制取二氧化碳,在完成实验后,对反应后的废液进行探究.他们取过滤后的废液100g,向其中逐渐滴加溶质的质量分数为10%的Na2CO3溶液,烧杯中溶液的质量与所滴入Na2CO3溶液的质量关系如图所示: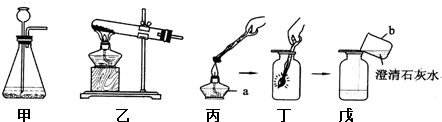
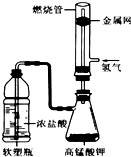 某化学课外活动小组用如图所示的装置制取氯气(Cl2)并模拟盐酸工业合成氯化氢(金属网用以防止气体在燃烧过程中发生爆炸).
某化学课外活动小组用如图所示的装置制取氯气(Cl2)并模拟盐酸工业合成氯化氢(金属网用以防止气体在燃烧过程中发生爆炸).