题目内容
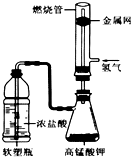 某化学课外活动小组用如图所示的装置制取氯气(Cl2)并模拟盐酸工业合成氯化氢(金属网用以防止气体在燃烧过程中发生爆炸).
某化学课外活动小组用如图所示的装置制取氯气(Cl2)并模拟盐酸工业合成氯化氢(金属网用以防止气体在燃烧过程中发生爆炸).查阅资料:常温下,氯气是一种浅绿色有毒气体.
氯气的制取:
(1)实验室可利用高锰酸钾固体与浓盐酸制取氯气,同时生成KCl、MnCl2和水.写出制取氯气反应的化学方程式为
2KMnO4+16HCl═2KCl+2MnCl2+8H2O+5Cl2↑
2KMnO4+16HCl═2KCl+2MnCl2+8H2O+5Cl2↑
.(2)将浓盐酸加入锥形瓶的操作方法是
将锥形瓶倾斜,标签向着手心,试剂瓶口与锥形瓶口紧挨着,倾倒即可
将锥形瓶倾斜,标签向着手心,试剂瓶口与锥形瓶口紧挨着,倾倒即可
.合成氯化氢:
(3)实验过程:①先通入氢气,先
验纯
验纯
后点燃;②待氢气稳定燃烧后,将浓盐酸加入锥形瓶中,氢气在氯气中持续安静燃烧.(4)氢气在氯气中燃烧的化学方程式是
H2+Cl2
2HCl
| ||
H2+Cl2
2HCl
,根据该实验,你对“物质燃烧的条件”的新认识是
| ||
燃烧不一定有氧气参加
燃烧不一定有氧气参加
.(5)观察到燃烧管的上方产生大量白雾,这是由于
氢气和氯气燃烧生成氯化氢,氯化氢与空气中水蒸气接触,氯化氢溶于水形成盐酸小液滴
氢气和氯气燃烧生成氯化氢,氯化氢与空气中水蒸气接触,氯化氢溶于水形成盐酸小液滴
.(6)先通氢气并点燃,再通氯气的原因是
先通氢气并点燃,利用氢气燃烧先将装置内氧气消耗,再使氢气和氯气燃烧
先通氢气并点燃,利用氢气燃烧先将装置内氧气消耗,再使氢气和氯气燃烧
;采用外管通氢气、内管通氯气的目的是氢气的密度比空气密度小,所以向上运动,且氢气无毒,氯气有毒,泄漏后污染环境,所以采用外管通氢气、内管通氯气
氢气的密度比空气密度小,所以向上运动,且氢气无毒,氯气有毒,泄漏后污染环境,所以采用外管通氢气、内管通氯气
.分析:(1)根据方程式的书写方法考虑;(2)根据液体药品的取用方法考虑;(3)根据点燃可燃性气体容易发生爆炸考虑;(4)根据方程式的书写和燃烧的反应物考虑;(5)根据氯化氢与空气中的水蒸气结合形成盐酸小液滴考虑;(6)利用氢气燃烧先将装置内氧气消耗,再使氢气和氯气燃烧,氢气的,密度比空气密度小,向上运动,与上方的氯气结合,发生反应.
解答:解:(1)反应物是高锰酸钾和氯化氢,生成物是氯化钾、氯化锰和水,用观察法配平即可,所以方程式是:2KMnO4+16HCl═2KCl+2MnCl2+8H2O+5Cl2↑;
(2)将锥形瓶倾斜,标签向着手心,试剂瓶口与锥形瓶口紧挨着,倾倒即可;
(3)点燃可燃性气体容易发生爆炸,所以点燃可燃性气体前,要检验气体的纯度,再点燃该气体;
(4)氢气在氯气中燃烧的反应物是氢气和氯气,生成物是氯化氢,用观察法配平即可,所以方程式是:H2+Cl2
2HCl;由该方程式可知燃烧不一定有氧气参加;
(5)氢气和氯气燃烧生成氯化氢,氯化氢与空气中水蒸气接触,氯化氢溶于水形成盐酸小液滴,所以观察到燃烧管的上方产生大量白雾;
(6)先通氢气并点燃,利用氢气燃烧先将装置内氧气消耗,再使氢气和氯气燃烧,由于氢气的密度比空气密度小,所以向上运动,且氢气无毒,氯气有毒,泄漏后污染环境,所以采用外管通氢气、内管通氯气.
故答案为:(1)2KMnO4+16HCl═2KCl+2MnCl2+8H2O+5Cl2↑;(2)将锥形瓶倾斜,标签向着手心,试剂瓶口与锥形瓶口紧挨着,倾倒即可;(3)验纯;(4)H2+Cl2
2HCl;燃烧不一定有氧气参加;(5)氢气和氯气燃烧生成氯化氢,氯化氢与空气中水蒸气接触,氯化氢溶于水形成盐酸小液滴;(6)先通氢气并点燃,利用氢气燃烧先将装置内氧气消耗,再使氢气和氯气燃烧;氢气的密度比空气密度小,所以向上运动,且氢气无毒,氯气有毒,泄漏后污染环境,所以采用外管通氢气、内管通氯气.
(2)将锥形瓶倾斜,标签向着手心,试剂瓶口与锥形瓶口紧挨着,倾倒即可;
(3)点燃可燃性气体容易发生爆炸,所以点燃可燃性气体前,要检验气体的纯度,再点燃该气体;
(4)氢气在氯气中燃烧的反应物是氢气和氯气,生成物是氯化氢,用观察法配平即可,所以方程式是:H2+Cl2
| ||
(5)氢气和氯气燃烧生成氯化氢,氯化氢与空气中水蒸气接触,氯化氢溶于水形成盐酸小液滴,所以观察到燃烧管的上方产生大量白雾;
(6)先通氢气并点燃,利用氢气燃烧先将装置内氧气消耗,再使氢气和氯气燃烧,由于氢气的密度比空气密度小,所以向上运动,且氢气无毒,氯气有毒,泄漏后污染环境,所以采用外管通氢气、内管通氯气.
故答案为:(1)2KMnO4+16HCl═2KCl+2MnCl2+8H2O+5Cl2↑;(2)将锥形瓶倾斜,标签向着手心,试剂瓶口与锥形瓶口紧挨着,倾倒即可;(3)验纯;(4)H2+Cl2
| ||
点评:解答本题关键是要知道方程式的书写方法:一写二配三注明四等号,知道氯化氢溶于水形成盐酸小液滴.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
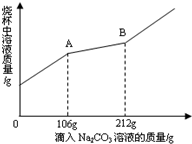 某化学课外活动小组用石灰石和稀盐酸为原料制取二氧化碳,在完成实验后,对反应后的废液进行探究.他们取过滤后的废液100g,向其中逐渐滴加溶质的质量分数为10%的Na2CO3溶液,烧杯中溶液的质量与所滴入Na2CO3溶液的质量关系如图所示:
某化学课外活动小组用石灰石和稀盐酸为原料制取二氧化碳,在完成实验后,对反应后的废液进行探究.他们取过滤后的废液100g,向其中逐渐滴加溶质的质量分数为10%的Na2CO3溶液,烧杯中溶液的质量与所滴入Na2CO3溶液的质量关系如图所示:
