题目内容
【题目】根据下列装置图回答问题。
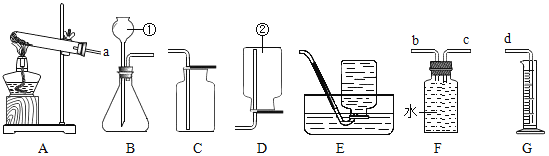
(1)标出仪器名称:①是_____;②是_____。
(2)实验室可以通过多种途径制得氧气,实验室若用氯酸钾和二氧化锰的混合物制取氧气,可选择的装置组合是_____(只写一组),有关反应的化学方程式为_____,氯酸钾中氯元素的化合价为_____。
(3)实验室用 5%的双氧水溶液在 MnO2 存在的条件下制氧气,此实验选 B 作为发生装置,为了能控制反应的速度,可以做何改进?_____;若用 E 装置收集氧气,当水中有气泡连续冒出时便开始收集,连续收集了三瓶气体,当用带火星的木条对三瓶气体进行检验时,发现第一瓶氧气不能使带火星的木条复燃,原因可能为_____。
A 开始瓶中没有装满水 B 收集了锥形瓶与导管中的空气
C 没有在水面下将瓶口盖好就将瓶子拿离水面 D 装置气密性不好
(4)小明同学准备做铁丝在氧气中燃烧的实验时,发现盛放氧气的集气瓶中没有放水,于是他揭开毛玻璃片,在水槽中舀了一点水继续实验。你认为他的操作正确吗,为什么?_____
(5)甲烷是密度小于空气,极难溶于水的气体。实验室用加热无水醋酸钠和碱石灰固体混合物的方法来制取。制取甲烷应选用的发生装置是_____(填序号),得到较纯净的甲烷可选用 F 装置进行排水法收集,如果甲烷从 b 端通入,请将图中导管补画完整_________。
【答案】长颈漏斗 集气瓶 AC(或AE) 2KClO3 2KCl+3O2↑ +5 将长颈漏斗改为分液漏斗; A.B.C 不正确,揭开毛玻璃加水氧气容易逸出,应移开一点点加水 A
2KCl+3O2↑ +5 将长颈漏斗改为分液漏斗; A.B.C 不正确,揭开毛玻璃加水氧气容易逸出,应移开一点点加水 A 
【解析】
(1)由图可知,仪器①的名称是长颈漏斗,故填长颈漏斗;
仪器②的名称是集气瓶,故填集气瓶。
(2)该反应的反应物氯酸钾和二氧化锰都是固体,反应条件是加热,应选择固体受热发生装置,即A,氧气不易溶于水,密度比空气大,可用排水法或向上排空气法收集,即C或E,故填AC或AE;
氯酸钾在二氧化锰作催化剂和加热的条件下反应生成氯化钾和氧气,故反应的化学方程式写为:2KClO3 2KCl+3O2↑;
2KCl+3O2↑;
氯酸钾中,钾元素显+1价,氧元素显﹣2价,设氯元素的化合价为x,根据化合物中各元素的化合价的代数和为零,则(+1)+x+(﹣2)×3=0,x=+5,故填+5。
(3)实验室用 5%的双氧水溶液在 MnO2 存在的条件下制氧气,此实验选 B 作为发生装置,为了能控制反应的速度,可将长颈漏斗改为分液漏斗,故填将长颈漏斗改为分液漏斗;
A 开始瓶中没有装满水造成收集的氧气不纯,选项错误;
B 没有等到导管口的气泡连续均匀冒出就开始收集,收集了锥形瓶与导管中的空气,选项错误;
C 没有在水面下将瓶口盖好就将瓶子拿离水面,选项错误;
D 导管口有气泡冒出,说明装置气密性好,选项正确,故填ABC。
(4)这种操作是错误的,揭开毛玻璃加水氧气容易逸出,应移开一点点加水,故填不正确,揭开毛玻璃加水氧气容易逸出,应移开一点点加水。
(5)实验室制取甲烷的反应物是固体,反应条件是加热,应选择固体受热发生装置,即A,故填A;
甲烷的密度比水小,所以甲烷应从短管进入,水从长管排出,故填 。
。

 阅读快车系列答案
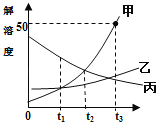
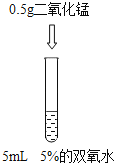
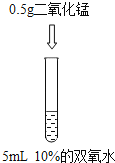
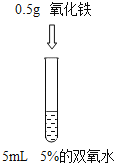
阅读快车系列答案【题目】为了探究”影响双氧水制氧气的速率”的因素,某学习小组设计了下列实验,下列说法正确的是( )
实验① | 实验② | 实验③ |
|
|
|
A. 对比实验②和③,可研究双氧水的质量分数对反应速率的影响
B. 对比实验①和②,可研究双氧水的质量分数对反应速率的影响
C. 对比实验②和③,可研究催化剂的种类对反应速率的影响
D. 对比实验①和②,可研究催化剂的种类对反应速率的影响
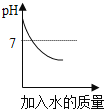
【题目】下列所示图象能正确反映对应的实验或事实的是( )
A | B | C | D | |
图象 |
|
|
|
|
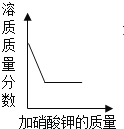
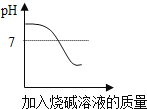
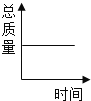
实验或事实 | 向pH等于12的氢氧化钙溶液不断加水稀释 | 20℃向一杯不饱和的KNO3溶液中逐步加入KNO3晶体 | 向稀盐酸中加入过量的烧碱溶液 | 将一定质量的碳在密闭容器中(含空气)加热 |
A. AB. BC. CD. D