题目内容
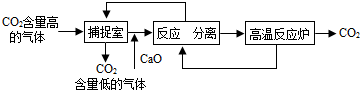
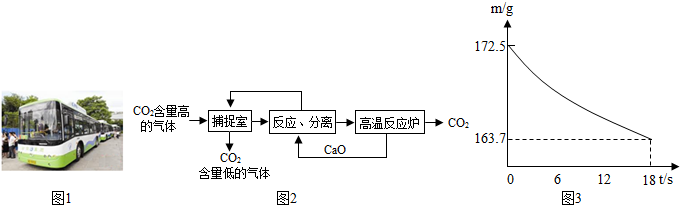
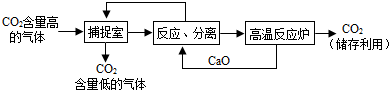
近来有科学家提出利用“碳捕捉技术”来降低工业生产中二氧化碳的排放量.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用.常利用足量的NaOH溶液来“捕捉”CO2,过程如下图所示(部分条件及物质未标出).
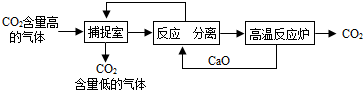
①捕捉室中发生反应的化学方程式为
②此反应中氧化钙俗称
③“反应分离”中,得到固体物质的基本操作是
④整个过程中,可以循环利用的物质有

①捕捉室中发生反应的化学方程式为
CO2+2NaOH=Na2CO3+H2O
CO2+2NaOH=Na2CO3+H2O
.②此反应中氧化钙俗称
生石灰
生石灰
,此物质溶于水的过程会放热
放热
(放热或吸热)③“反应分离”中,得到固体物质的基本操作是
过滤
过滤
,该固体是碳酸钙.④整个过程中,可以循环利用的物质有
氢氧化钠和氧化钙
氢氧化钠和氧化钙
.分析:根据二氧化碳与氢氧化钠反应的反应物、生成物写出化学方程式;生石灰可与水反应,并放出大量的热;过滤是将固体和液体分离的方法,据流程图分析可循环利用的物质.
解答:解:①捕捉室中发生反应的化学反应是二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,化学方程式为CO2+2NaOH=Na2CO3+H2O;
故填:CO2+2NaOH=Na2CO3+H2O;
②氧化钙俗称生石灰,CaO和水反应生成氢氧化钙并放出大量的热;
故填:生石灰;放热;
③固体与液体分开用过滤;
故填:过滤;
④碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,氢氧化钠又是捕捉室中的反应物,所以可以循环利用;碳酸钙高温生成氧化钙和二氧化碳,观察图示,氧化钙还可循环利用,氧化钙和氢氧化钠都可以循环利用;
故填:氢氧化钠和氧化钙.
故填:CO2+2NaOH=Na2CO3+H2O;
②氧化钙俗称生石灰,CaO和水反应生成氢氧化钙并放出大量的热;
故填:生石灰;放热;
③固体与液体分开用过滤;
故填:过滤;
④碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,氢氧化钠又是捕捉室中的反应物,所以可以循环利用;碳酸钙高温生成氧化钙和二氧化碳,观察图示,氧化钙还可循环利用,氧化钙和氢氧化钠都可以循环利用;
故填:氢氧化钠和氧化钙.
点评:此题是对物质的性质和流程图的分析,注重对学生解读解能力的考查,有利于培养学生的探究能力.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目