题目内容
(2012?浦口区二模)“低碳城市”的理念贯穿在上海世博园的建设中
(1)“低碳城市”的建设减少了二氧化碳气体的排放,能减缓
(2)法国化学家PaulSabatier采用“组合转化”技术使CO2和H2在催化剂作用下生成CH4和H2O.试写出该反应的化学方程式
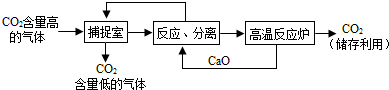
(3)近来有科学家提出利用“碳捕捉技术”来降低工业生产中二氧化碳的排放量.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用.常利用足量的NaOH溶液来“捕捉”CO2,过程如图所示(部分条件及物质未标出).①捕捉室中发生反应的化学方程式为:
②把CaO放入反应分离室中与H2O反应,请写出该反应的化学方程式:
③“反应分离”中,得到固体物质的基本操作是
④整个过程中,可以循环利用的物质有
(4)取10g碳酸钙固体高温加热,一段时间后停止加热,测得剩余固体中钙元素的质量分数为50%,则下列判断正确的是
A.生成了2g二氧化碳
B.剩余固体质量为5g
C.生成了5.6g氧化钙
D.剩余碳酸钙的质量为8g.

(1)“低碳城市”的建设减少了二氧化碳气体的排放,能减缓
温室效应
温室效应
的程度;自然界中消耗二氧化碳的主要途径是光合作用
光合作用
;请你写出一种日常生活中符合“低碳经济”理念的做法:随手关灯,废物利用
随手关灯,废物利用
.(2)法国化学家PaulSabatier采用“组合转化”技术使CO2和H2在催化剂作用下生成CH4和H2O.试写出该反应的化学方程式
CO2+4H2
CH4+2H2O?
| ||
CO2+4H2
CH4+2H2O?
.
| ||
(3)近来有科学家提出利用“碳捕捉技术”来降低工业生产中二氧化碳的排放量.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用.常利用足量的NaOH溶液来“捕捉”CO2,过程如图所示(部分条件及物质未标出).①捕捉室中发生反应的化学方程式为:
?CO2+2NaOH═Na2CO3+H2O
?CO2+2NaOH═Na2CO3+H2O
.②把CaO放入反应分离室中与H2O反应,请写出该反应的化学方程式:
CaO+H2O═Ca(OH)2
CaO+H2O═Ca(OH)2
;利用此反应,氧化钙可用作食品干燥
干燥
剂.③“反应分离”中,得到固体物质的基本操作是
过滤
过滤
,该固体是碳酸钙.④整个过程中,可以循环利用的物质有
CaO、NaOH
CaO、NaOH
.(4)取10g碳酸钙固体高温加热,一段时间后停止加热,测得剩余固体中钙元素的质量分数为50%,则下列判断正确的是
A
A
.A.生成了2g二氧化碳
B.剩余固体质量为5g
C.生成了5.6g氧化钙
D.剩余碳酸钙的质量为8g.
分析:二氧化碳在大气中的含量增多,导致冰川融化、海平面升高、土地干旱等一系列气候问题,这就是由二氧化碳等气体形成的温室效应而造成的.二氧化碳,是温室效应的罪魁祸首,“低碳城市”的建设就得减少CO2 气体大的排放;在自然界中消耗二氧化碳的主要途径是通过植物的光合作用;在日常生活中符合“低碳经济“理念的做法很多,如提倡骑自行车、步行、乘公交等;采用“组合转化“技术使CO2和H2在催化剂作用下生成CH4和H2O,配平即可;二氧化碳与碱的反应;生石灰的性质等;有关的计算要准确.
解答:解:(1)二氧化碳,是温室效应的罪魁祸首,“低碳城市”的建设就得减少CO2 气体大的排放;在自然界中消耗二氧化碳的主要途径是通过植物的光合作用;在日常生活中符合“低碳经济“理念的做法很多,如提倡骑自行车、步行、乘公交等;故答案为:温室效应;光合作用;随手关灯,废物利用(合理即可);
(2)用“组合转化“技术使CO2和H2在催化剂作用下生成CH4和H2O,配平即可;故答案为:CO2+4H2
CH4+2H2O
(3)二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,配平即可;CaO和水反应生成氢氧化钙,因此氧化钙可以做干燥剂;固体与液体分开用过滤;整个过程中,可以循环利用的物质有氧化钙和氢氧化钠;故答案为:①CO2+2NaOH═Na2CO3+H2O;②CaO+H2O═Ca(OH)2;干燥;③过滤;④CaO、NaOH
(4)10g碳酸钙中含钙元素的质量=10g×
=4g,反应一段时间后停止加热,剩余固体的质量=4g÷50%=8g,根据质量守恒定律:二氧化碳的质量=10g-8g=2g,故答案为:A
(2)用“组合转化“技术使CO2和H2在催化剂作用下生成CH4和H2O,配平即可;故答案为:CO2+4H2
| ||
(3)二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,配平即可;CaO和水反应生成氢氧化钙,因此氧化钙可以做干燥剂;固体与液体分开用过滤;整个过程中,可以循环利用的物质有氧化钙和氢氧化钠;故答案为:①CO2+2NaOH═Na2CO3+H2O;②CaO+H2O═Ca(OH)2;干燥;③过滤;④CaO、NaOH
(4)10g碳酸钙中含钙元素的质量=10g×
| 40 |
| 100 |
点评:本考点考查了碳的循环、温室效应、碱的性质和化学方程式的书写等,低碳生活、低碳经济是当前十分热门的话题,我们每个公民都应该从自己做起,从力所能及的事情做起,为保护环境出一份力.本题综合性比较强,要加强记忆,理解应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 (2012?浦口区二模)如图为两种物质在水中的溶解度曲线.下列说法正确的是( )
(2012?浦口区二模)如图为两种物质在水中的溶解度曲线.下列说法正确的是( ) (2012?浦口区二模)某校课外活动小组的同学们利用水的电解实验探究水的组成,他们量取192.7mL水(水的密度为1.00g/cm3),并向水中加入了7.3g氢氧化钠固体,充分溶解后按图所示的装置进行实验,接通电源,当A管收集到22.3mL气体(气体密度为0.09g/L)时,停止实验.请分析回答:
(2012?浦口区二模)某校课外活动小组的同学们利用水的电解实验探究水的组成,他们量取192.7mL水(水的密度为1.00g/cm3),并向水中加入了7.3g氢氧化钠固体,充分溶解后按图所示的装置进行实验,接通电源,当A管收集到22.3mL气体(气体密度为0.09g/L)时,停止实验.请分析回答: