题目内容
“低碳城市”的理念贯穿在上海世博园的建设中.
(1)“低碳城市”的建设减少了二氧化碳气体的排放,能减缓
(2)法国化学家PaulSabatier采用“组合转化”技术使CO2和H2在催化剂作用下生成CH4和H2O.试写出该反应的化学方程式
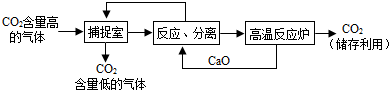
(3)近来有科学家提出利用“碳捕捉技术”来降低工业生产中二氧化碳的排放量.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用.常利用足量的NaOH溶液来“捕捉”CO2,过程如图所示(部分条件及物质未标出).

①捕捉室中发生反应的化学方程式为:
②把CaO放入反应分离室中与H2O反应,请写出该反应的化学方程式:
③“反应分离”中,得到固体物质的基本操作是
(1)“低碳城市”的建设减少了二氧化碳气体的排放,能减缓
温室效应
温室效应
的程度;自然界中消耗二氧化碳的主要途径是植物的光合作用
植物的光合作用
;请你写出一种日常生活中符合“低碳经济”理念的做法:研制和开发新能源替代传统能源等
研制和开发新能源替代传统能源等
.(2)法国化学家PaulSabatier采用“组合转化”技术使CO2和H2在催化剂作用下生成CH4和H2O.试写出该反应的化学方程式
CO2+4H2
CH4+2H2O
| ||
CO2+4H2
CH4+2H2O
.?
| ||
(3)近来有科学家提出利用“碳捕捉技术”来降低工业生产中二氧化碳的排放量.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用.常利用足量的NaOH溶液来“捕捉”CO2,过程如图所示(部分条件及物质未标出).

①捕捉室中发生反应的化学方程式为:
CO2+2NaOH═Na2CO3+H2O
CO2+2NaOH═Na2CO3+H2O
.②把CaO放入反应分离室中与H2O反应,请写出该反应的化学方程式:
CaO+H2O═Ca(OH)2
CaO+H2O═Ca(OH)2
.③“反应分离”中,得到固体物质的基本操作是
过滤
过滤
,该固体是碳酸钙.分析:(1)“低碳城市”的建设要减少CO2气体的排放;在自然界中消耗二氧化碳的主要途径是通过植物的光合作用,可以从节电、节能和回收等环节来改变生产细节,据此进行分析解答.
(2)CO2和H2在催化剂作用下生成CH4和H2O,写出反应的化学方程式即可.
(3)①根据题意,常利用足量的NaOH溶液来“捕捉”二氧化碳,写出反应的化学方程式即可.
②氧化钙与水反应生成氢氧化钙,写出反应的化学方程式即可.
③反应分离是将碳酸钙与氢氧化钠溶液分离,过滤是将固体和液体分离的一种方法.
(2)CO2和H2在催化剂作用下生成CH4和H2O,写出反应的化学方程式即可.
(3)①根据题意,常利用足量的NaOH溶液来“捕捉”二氧化碳,写出反应的化学方程式即可.
②氧化钙与水反应生成氢氧化钙,写出反应的化学方程式即可.
③反应分离是将碳酸钙与氢氧化钠溶液分离,过滤是将固体和液体分离的一种方法.
解答:解:(1)二氧化碳是温室效应的罪魁祸首,“低碳城市”的建设就得减少CO2气体的排放,能减缓温室效应的程度;自然界中消耗二氧化碳的主要途径是通过植物的光合作用;在日常生活中符合“低碳经济“理念的做法很多,如研制和开发新能源替代传统能源,优化建筑设计,增强室内自然采光,减少照明用电等
(2)CO2和H2在催化剂作用下生成CH4和H2O,反应的化学方程式为:CO2+4H2
CH4+2H2O.
(3)①常利用足量的NaOH溶液来“捕捉”二氧化碳,二氧化碳与氢氧化钠反应生成碳酸钠和水,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O.
②氧化钙与水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2.
③碳酸钠与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠溶液,“反应分离”中得到固体物质是碳酸钙,采用的是过滤的方法.
故答案为:(1)温室效应;植物的光合作用;研制和开发新能源替代传统能源等;(2)CO2+4H2
CH4+2H2O;(3)①CO2+2NaOH═Na2CO3+H2O;②CaO+H2O═Ca(OH)2;③过滤.
(2)CO2和H2在催化剂作用下生成CH4和H2O,反应的化学方程式为:CO2+4H2
| ||
(3)①常利用足量的NaOH溶液来“捕捉”二氧化碳,二氧化碳与氢氧化钠反应生成碳酸钠和水,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O.
②氧化钙与水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2.
③碳酸钠与氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠溶液,“反应分离”中得到固体物质是碳酸钙,采用的是过滤的方法.
故答案为:(1)温室效应;植物的光合作用;研制和开发新能源替代传统能源等;(2)CO2+4H2
| ||
点评:本题难度不大,掌握自然界的碳循环、二氧化碳的化学性质、氧化钙的化学性质、化学方程式的书写等并能灵活运用是正确解答本题的关键.

练习册系列答案
 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目