题目内容
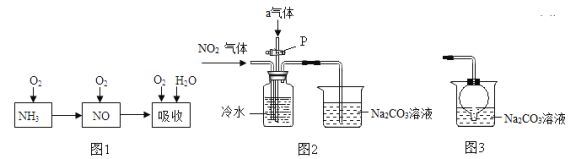
【题目】如图是工业上利用含SO2的烟气制备咬K2SO4的流程。

相关物质的溶解度如下表所示:
物质 | KCl | K2SO4 | NH4Cl | (NH4) 2SO4 |
溶解度/( 25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(1)在“脱硫”反应中,CaCO3粉碎后与水混合成 (填“溶液”、“悬浊液”或“乳浊液”)后,与含SO2的烟气、空气中气体反生成石膏( CaSO4·2H2O ),写出该反应的化学方程式: 。
(2)石膏与饱和(NH4) 2CO3溶液相混合,发生反应I时需不断搅拌,其目的是 。
(3)“操作I”的名称是 ,实验室进行该操作时所用到的玻璃仪器有烧杯、玻璃棒、 。
(4)你认为反应II在常温下能实现的原因是 。
(5)NH4C1在农业上可以用作化肥,从NH4C1溶液中得到NH4C1晶体,可以采用加热浓缩、 、过滤的方法。
(6)此工艺流程中可以循环利用的物质是 。
【答案】(1)悬浊液 2CaCO3+ 2SO2+ O2+ 4H2O== 2CaSO4·2H2O CaCl2+2CO2
(2)使原料充分反应,提高原料利用率 (3)过滤 漏斗
(4)常温下K2SO4的溶解度较小 (5)冷却结晶 (6)CaCO3
【解析】
试题分析:(1)CaCO3不溶于水,粉碎后与水混合悬浮在水中,静置后会下沉,故形成的混合形式是悬浊液;CaCO3与水混合下沉的悬浊液与含SO2的烟气、空气中气体反生成石膏( CaSO4·2H2O ) ,化学方程式为:2CaCO3+ 2SO2+ O2+ 4H2O== 2CaSO4·2H2O CaCl2+2CO2
(2)石膏与饱和(NH4) 2CO3溶液相混合,发生反应I时需不断搅拌,其目的是:使原料充分反应,提高原料利用率
(3)“操作I”是将固体和液体分离,名称是过滤;实验室进行该操作时所用到的玻璃仪器有:烧杯、玻璃棒、漏斗
(4)反应II发生的复分解反应,根据复分解反应发生的条件:生成物中要有沉淀、气体或水生成,故该反应在常温下能实现的原因是:根据表格中提高的数据:常温下K2SO4的溶解度较小,会以沉淀的形式解析析出
(5)NH4C1在农业上可以用作化肥,从NH4C1溶液中得到NH4C1晶体,可以采用加热浓缩、冷却结晶,再过滤的方法
(6)根据流程图,此工艺流程中可以循环利用的物质是CaCO3

 阅读快车系列答案
阅读快车系列答案【题目】只用下列鉴别方法不能把待鉴别的物质区分开的是
选项 | 待鉴别的物质 | 鉴别方法 |
A | 二氧化碳和氮气 | 分别向其中伸入燃着的木条,观察燃烧情况 |
B | 硬水和软水 | 加肥皂水,振荡,观察产生泡沫情况 |
C | 过氧化氢溶液和水 | 加二氧化锰,观察有无气泡产生 |
D | 氧气和空气 | 分别向其中伸入燃着的木条,观察燃烧情况 |
【题目】下列各组物质能按照关系图![]() (“→”表示反应一步完成)相互转化的是( )
(“→”表示反应一步完成)相互转化的是( )
X | Y | Z | |
A | Cu | CuO | Cu(OH)2 |
B | Ca(OH)2 | Ca(NO3)2 | CaCl2 |
C | Fe2O3 | Fe | FeSO4 |
D | Na2CO3 | NaOH | Na2SO4 |