题目内容
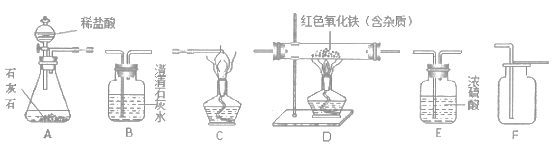
【题目】CO在高温下还原Fe2O3的化学方程式为___________________;在该实验中常用澄清的石灰水检验反应生成的气体,其原理用化学方程式可表示为______________________;实验装置后端常放置一个燃着的酒精灯,其作用是______________。
【答案】3CO+Fe2O3![]() 2Fe+3CO2 Ca(OH)2 +CO2 = CaCO3↓+H2O 点燃尾气,防止一氧化碳气体污染空气
2Fe+3CO2 Ca(OH)2 +CO2 = CaCO3↓+H2O 点燃尾气,防止一氧化碳气体污染空气
【解析】
CO在高温下还原Fe2O3,原理是氧化铁和一氧化碳在高温条件下反应生成铁和二氧化碳,化学方程式为3CO+Fe2O3![]() 2Fe+3CO2;在该实验中常用澄清的石灰水检验反应生成的气体,其原理是二氧化碳和氢氧化钙梵音生成碳酸钙沉淀和水,化学方程式可表示为Ca(OH)2 +CO2 = CaCO3↓+H2O;炼铁装置的尾气的成分是生成的二氧化碳和剩余的一氧化碳,依据一氧化碳燃烧生成二氧化碳,实验装置后端常放置一个燃着的酒精灯,其作用是点燃尾气,防止一氧化碳气体污染空气。
2Fe+3CO2;在该实验中常用澄清的石灰水检验反应生成的气体,其原理是二氧化碳和氢氧化钙梵音生成碳酸钙沉淀和水,化学方程式可表示为Ca(OH)2 +CO2 = CaCO3↓+H2O;炼铁装置的尾气的成分是生成的二氧化碳和剩余的一氧化碳,依据一氧化碳燃烧生成二氧化碳,实验装置后端常放置一个燃着的酒精灯,其作用是点燃尾气,防止一氧化碳气体污染空气。

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案【题目】硝酸钾的部分溶解度数据见下表。
温度(℃) | 10 | 20 | 40 | 60 |
溶解度(g/100g 水) | 20.9 | 31.6 | 63.9 | 110 |
①20℃时,称取 10.0 克硝酸钾固体加入到 40 克水中,用_____(写出仪器名称)搅拌,充分溶解后得到_____(选填“饱和”或“不饱和”)溶液。
②将上述溶液升温至 60℃,所得溶液的溶质质量分数为_____。
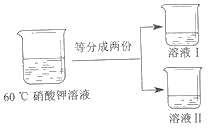
③将 60℃的硝酸钾溶液进行如图所示操作。
将溶液 I 降温,开始析出硝酸钾晶体的温度介于_____℃(选填编号之间。
A. 40-60 B. 20-40 C. 10-20 D. 低于 10
为得到 60℃时硝酸钾饱和溶液,将溶液 II 恒温蒸发 15 克水,请分析该操作能否达到实验目的并说明理由_____。
【题目】对下列事实的微观解释正确的是![]()
![]()
选项 | 事实 | 解释 |
A | 体温计中的水银 | 分子间间隔随温度改变 |
B | 氧气能压缩在蓝色钢瓶中 | 氧分子大小随压强变大而减小 |
C | 金刚石、石墨性质存在明显差异 | 碳原子的排列方式不同 |
D | 氮气是无色的 | 氮分子是无色的 |
A. AB. BC. CD. D