题目内容
【题目】下图是甲、乙两种固体物质的溶解度曲线。下列说法正确的是( )
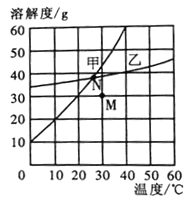
A. 40℃时,甲物质饱和溶液溶质的质量分数为60%
B. N点状态的甲、乙两种溶液中溶质的质量相等
C. 当乙中含有少量的甲,可用降温结晶法提纯乙
D. M点状态的甲溶液通过降温并加入甲物质可转化为N点状态
【答案】D
【解析】
A、40℃时,甲的溶解度为60g,40℃时,饱和溶液溶质的质量分数=![]() ,故A错误;
,故A错误;
B、 N点状态是某温度下,甲、乙两种饱和溶液,由于没有确定溶液的质量,不能确定溶液中溶质的质量,故B错误;
C、 甲、乙的溶解度都随温度降低而降低,甲的溶解度受温度影响较大,乙的溶解度受温度影响较小,当乙中含有少量的甲,可用蒸发结晶法提纯乙,故C错误;
D、 M点状态是30℃时甲的不饱和溶液,N点状态是30℃时甲的饱和溶液,M点状态通过降温并加入甲物质可转化为N点状态,故D正确。故选D。

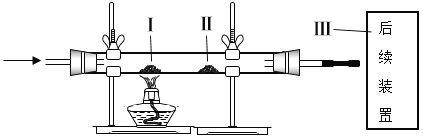
【题目】为探究影响氯酸钾分解速率的因素,小红同学把实验温度恒定在330℃或380℃,(其他实验条件见下表),并设计了以下实验。
实验编号 | 氯酸钾的质量 | 其他物质的质量∕g | 温度∕℃ | 收集氧气的体积/mL | 反应所需时间∕s |
① | 2.0 | 330 | 100 | t1 | |
② | 2.0 | CuO 0.5 | 330 | 100 | t2 |
③ | 2.0 | MnO2 0.5 | 330 | 100 | t3 |
④ | 2.0 | MnO2 ____ | _______ | 100 | t4 |
请回答
(1)进行实验②和③,并对对比,其实验目的是____________________。
(2)要说明氧化铜对氯酸钾分解速率的影响,则要选用实验______和实验_______进行对比。
(3)用实验③和④探究温度对氯酸钾分解速率的影响,则MnO2的质量是__________g,反应的温度是_________℃,实验④发生反应的化学方程式为___________________;若t3>t4,氯酸钾分解速率与温度的关系是__________________。
【题目】化学兴趣小组做酸和碱的中和反应时,往NaOH溶液中滴入几滴酚酞溶液,发现溶液刚变
红瞬间又褪成无色。讨论并猜想。
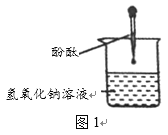
猜想一:可能是酚酞溶液变质
猜想二:可能与NaOH溶液的浓度有关
猜想三:可能是酚酞溶液在滴入过程中被O2氧化
……
(1)甲同学认为猜想一是不对的。其理由是_________________________。
(2)取3mL不同浓度的NaOH溶液,分别滴入3滴酚酞溶液,观察现象。得到NaOH溶液的浓度与酚酞溶液褪色时间关系如图2所示。
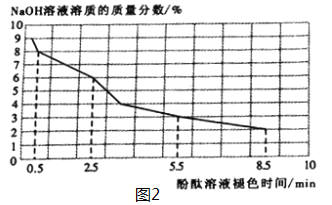
①根据图2所示,NaOH溶液溶质的质量分数________,酚酞溶液由红色褪为无色的时间越短。
②做酸和碱的中和反应时,滴加酚酞溶液的目的是________________________________。若用做实验的NaOH溶液溶质的质量分数为4%,完成该实验的操作时间应控制在_______之内。
(3)请设计实验,验证猜想三是否正确。
实验操作 | 实验现象 | 实验结论 |
__________ | 5.5min酚酞溶液褪色 | 酚酞溶液先变红后褪色与O2_______ (选填“有关”或“无关”) |
(4)探究酸碱中和反应时,逐滴加入稀盐酸的过程,并不断搅拌的目是_________________,写出该反应的化学方程式___________________________。