题目内容
【题目】某研究小组对过氧化氢溶液制取氧气进行如下探究。
实验一、探究H2O2质量分数、溶液pH、温度对反应速率的影响。设计如下表实验方案:
实验序号 | H2O2质量分数% | PH | 温度/℃ | 每分钟气泡数 |
1 | 30 | 5 | 20 | |
2 | 30 | 6 | 20 | |
3 | 30 | 11 | 20 | |
4 | 30 | 11 | a | |
5 | b | 11 | 20 |
试分析表中a、b的数值分别是a=__________________,b=______________________。
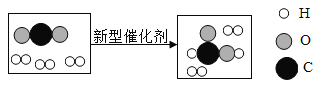
实验二、探究制取氧气的适宜催化剂。设计如下方案:
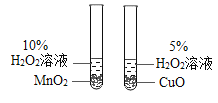
I.用MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
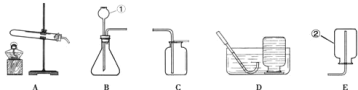
II.取30粒含MnO2的海藻酸钠微球,采用图1装置进行实验。改用其他三种微球,分别重复上述实验,得到如图2的锥形瓶内压强随时间变化的曲线图。
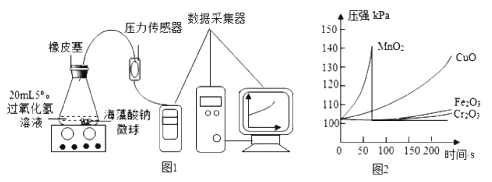
①每次实验时,海藻酸钠微球数应相同的原因是___________________________。
②用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因可能是______________________。
③从实验曲线看,催化效果较好、反应温和的催化剂是____________________。
【答案】15 20 确保催化剂用量一致,便于对比 产生气体速率过快,导致气压过大,橡皮塞被弹出( 或取下橡皮塞) CuO
【解析】
实验一:按照对照实验唯一变量的原则,依此进行实验设计。从1、3可以看出改变pH对反应速率的影响,3、4、5测定温度和过氧化氢质量分数对反应速率的影响,3和4进行对照实验,即可将温度作为变量,此时a不能等于20,所以可以为15或者25,只要不等于20,合理即可;3、5对照即可,此时b不等于30即可,可以为20或者25,合理即可;所以a=15,b=20。
实验二:①为了只改变催化剂不同这个变量,所以需要保证其他实验条件一致,因此要确保加入催化剂的质量相同,以便进行对比实验,故原因是确保催化剂用量一致,便于对比;
②装置是密闭的,氧气增加越快内部压强越大,造成压强瞬间增大,橡胶塞会被弹出,此时外界空气与瓶内相连,变为外界大气压,数据显示也符合外界大气压数值。此外若是人为将橡胶塞取下,也会出现类似情况,所以出现此种现象原因为:橡皮塞被弹出,或取下橡皮塞;
③二氧化锰压强增大最快,反应速率过快,氧化铁和氧化铬压强变化不大,催化效果不明显,只有氧化铜压强增大速度较为缓和,压强增大比较平稳,所以最佳催化剂为氧化铜。

【题目】木糖醇是一种白色粉末状固体,易溶于水,新型甜味剂,目前木塘醇口香糖正在取代蔗糖口香糖,是蔗糖和葡萄糖替代品。
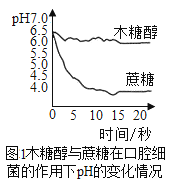
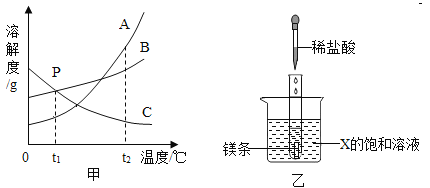
探究一:人们食用含糖量较高的物质会在口腔中细菌作用下产生酸性物质,腐蚀牙齿,形成龋齿。由图1判断食用_____(填“蔗糖”或“木塘醇”)能有效的防止龋齿。
探究二:[提出猜想]木糖醇由什么元素组成?
[进行实验]小晴取适量的木糖醇按如图2进行操作:
操作 | 现象 | 结论 |
①把木糖醇灼烧,将一干冷的烧杯罩在火焰上方 | 烧杯内壁有水雾 | 木糖醇中含有氢元素 |
②将_____罩在灼烧的木糖醇的火焰上方 | _____。 | 木糖醇中含有碳元素 |
[讨论交流]其他同学认为小睛的实验设计不严谨,原因是_____。
经改进实验后,检验到木糖醇在氧气中充分燃烧的产物只有二氧化碳和水,由此确定木糖醇中一定含有_____元素。
[继续探究]为进步确定其元素组成。利用如图3进行实验。(已知:装置中C中的氧化铜能确保木糖醇中的碳元素完全转化为二氧化碳;氢氧化钠固体可吸收水蒸气和二氧化碳)
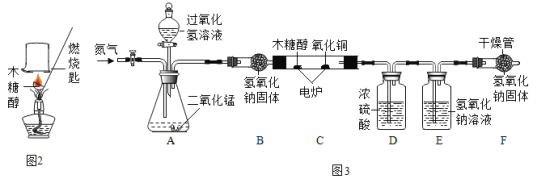
(1)实验前要通一会儿氮气,目的是_____。
(2)A装置中发生反应的化学方程式为_____。
[数据记录]6.08 g木糖醇在C装置中充分燃烧后,D装置增重4.32 g,E装置增重8.8 g。(产物被完全吸收)
[分析与讨论]数据6.08g木塘醇中氧元素的质量为_____g,由此可以确定木糖醇是由碳、氢、氧元素组成。
[反思评价]若没有F装置,对氧元素质量测定结果的影响是_____。(填“偏大”“偏小”或“无影响”)。