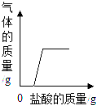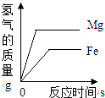题目内容
【题目】许多化学反应都伴随着明显的现象。但也有一些观察不到明显现象。请回答下列问题:
(1)向FeCl3溶液中滴加NaOH溶液,出现的明显现象是 。
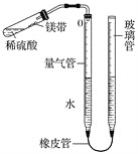
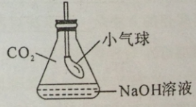
(2)CO2与NaOH溶液的反应无明显现象。为证明二者发生了反应,小红同学设计了如图所示的实验。向一盛满CO2气体的锥形瓶中注入一定量的NaOH溶液,迅速塞紧橡皮塞(胶塞中插有一下端系小气球的玻璃管)。然后振荡锥形瓶,会观察到小气球逐渐胀大,其主要原因是 。
(3)盐酸与NaOH溶液的中和反应也无明显现象,为证明二者确实发生了化学反应,在向NaOH溶液中滴加盐酸前,应先向NaOH溶液中滴入少许 。
【答案】(1)有红褐色的沉淀生成(2)CO2与NaOH反应,导致锥形瓶内的气压小雨外界大气压(3)无色酚酞试液或紫色石蕊试液或其他酸碱指示剂
【解析】三氯化铁可与氢氧化钠反应,生成红褐色的氢氧化铁沉淀;氢氧化钠溶液可以与二氧化碳发生反应,吸收二氧化碳,使得锥形瓶内的气体压强变小,外界大气进入小气球,使其胀大;酸碱中和反应没有明显现象,可借助酸碱指示剂来判断反应的发生以及进行的程度,如题可向氢氧化钠溶液中滴入几滴酚酞。

【题目】科学探究是学习化学重要而有效的学习方法。某校化学兴趣小组的同学以酸为专题,对酸的五种化学性质进行探究、总结及应用,请回答有关问题:
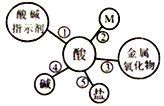
(1)酸的化学性质①一一酸与酸碱指示剂的作用。酸能使紫色石蕊溶液变成红色,不能使无色酚酞溶液变色。
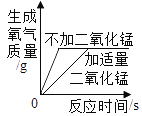
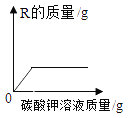
(2)酸的化学性质②,图中M所代表的物质类别是_______。黄金是一种常见饰品,现实生活中,少数商贩用黄铜冒充黄金出售,可以用化学的方法加以鉴别。某同学为了测定黄铜(铜锌合金)样品的成分,将60g稀HCl分三次加入到盛有10g该样品的烧杯中,所得数据如下表,则该黄铜样品中含锌的质量分数为___________。
实验次数 物质质量 | 第1次 | 第2次 | 第3次 |
加入稀盐酸质量/ g | 20 | 20 | 20 |
充分反应后剩余固体质量/g | 8.7 | 7.4 | 6.4 |
(3)酸的化学性质③一一酸与金属氧化物的反应。盐酸可用于金属制品表面除锈等。
(4)酸的化学性质④一一酸碱中和反应。
该校化学兴趣小组的同学重点以“酸碱中和反应”为课题进行探究。小宇同学向烧杯中的氢氧化钠溶液中滴加稀硫酸,一会儿后发现忘了滴加酸碱指示剂,于是他停止滴加稀硫酸。同学们纷纷对实验烧杯溶液中含有哪些溶质展开了讨论。
[提出问题]实验的烧杯中溶质含有哪些物质?
[提出猜想]猜想一 :溶质中只有Na2SO4
猜想二:溶质中可能是Na2SO4和NaOH
猜想三:溶质中可能是____________________。
[查阅资料] Na2SO4溶液呈中性
[实验探究]小宇同学设计如下的实验方案
方法步骤 | 实验现象 | 实验结论 | |
方案一 | 取少量烧杯中的溶液于洁净的试管中, 滴入几滴无色酚酞溶液 | 酚酞不变红色 | 猜想一正确 猜想二不正确 |
方案二 | 取少量烧杯中的溶液于洁净的试管中, 滴加BaCl2溶液 | 出现白色沉淀 | 猜想三正确 |
方案三 | 取少量烧杯中的溶液于洁净的试管中,入少量的黑色CuO粉末,振荡 | _________ | 猜想三正确 |
[方案评价]同学们对小宇上述的方案讨论后认为:
①方案一存在缺陷,该方案不能证明猜想一是正确的,其原因是____________________。
②方案二也不能证明猜想三是正确的,理由是__________________________________。
③同学们经过讨论,一致认为方案三能够证明猜想三是正确的,并讨论除此方案外,还可以向烧杯的溶液中加入活泼金属、碳酸盐等物质进行证明。
[实验反思]在分析化学反应后所得物质成分时,还需考虑反应物的用量。
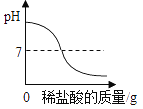
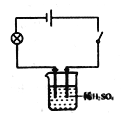
[学科渗透]如图所示,小宇同学在进行溶液导电性的实验时,将电极两端插入稀H2SO4溶液中,闭合开关,小灯泡正常发光,然后逐滴向稀H2SO4中加入Ba(OH)2溶液至过量,请推测小灯泡的发光情况为__________________;发生反应的化学方程式是___________。
(5)酸的化学性质⑤一一酸与盐的反应
利用下图所示装置来验证CO2气体的性质,要证明CO2与NaOH溶液能够发生反应,可先加氢氧化钠溶液,再加盐酸,气球的变化是_____________。
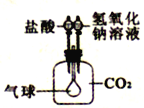
[方法感悟]在化学实验中,可通过验证反应后生成物的存在,来验证某化学反应的发生。
【题目】在一支试管中放入一小段镁条(已擦去氧化膜),再向试管中加入一定量的盐酸,镁条表面有_____产生,反应的化学方程式是_____。
[发现问题]为了再次观察上述反应现象,小林同学用较长的镁条重做上述实验,但发现了异常现象,试管中出现了白色沉淀。
[实验验证1]小林同学针对两次实验的不同,设计对比实验方案,探究出现异常现象的原因。
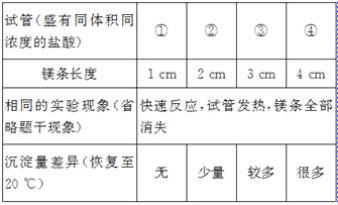
[得出结论]镁条与盐酸反应产生白色沉淀与_____有关。
[追问]白色沉淀是什么物质?
[查阅资料]①20 ℃时,100 g水中最多能溶解氯化镁54.8 g;
②镁能与热水反应产生一种碱和氢气;
③氯化银既不溶于水也不溶于稀硝酸。
[做出猜想]猜想一:镁;猜想二:氯化镁;猜想三:氢氧化镁,猜想的依据是_____(用化学方程式表示)。
[实验验证2]将白色沉淀洗涤干净,分别取少量沉淀于A、B、C试管中,进行如表实验:
试管 | 操作 | 现象 | 结论 |
A | 加入足量盐酸 | _____,白色沉淀_____ | 猜想一不正确,但这种白色沉淀能溶于盐酸 |
B | 加入足量水 | 白色沉淀_____ | 猜想二不正确 |
C | 加入适量稀硝酸 | 白色沉淀消失 | 原白色沉淀中含有的离子是:Mg2+、_____ |
继续滴加几滴硝酸银溶液 | 出现大量白色沉淀 |