题目内容
(3分)孔雀石的主要成分为碱式碳酸铜[Cu2 (OH) 2CO3],化学小组的同学利用 Cu2 (OH) 2CO3+4HCl="2" CuCl2+CO2↑+3H2O,测定某孔雀石中碱式碳酸铜的质量分数。称取该铜矿样品30g于烧杯中,逐滴加入溶质质量分数为10%的稀盐酸至恰好完全反应,共用去稀盐酸146g(假设铜矿中的其他成分不与稀盐酸反应,也不溶于水)。则该孔雀石样品中碱式碳酸铜的质量分数是多少?反应后所得溶液中溶质的质量分数是多少?
74%; 16.5%
Cu2 (OH) 2CO3 + 4HCl = 2 CuCl2 + CO2↑ + 3H2O
222 146 270 44 54
X 146g×10% y z ……………1分
X=22.2g
Y=27g
Z=4.4g
Cu2 (OH) 2CO3%=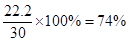 …………………………………………1分
…………………………………………1分
C%= …………………………………………1分
…………………………………………1分
222 146 270 44 54
X 146g×10% y z ……………1分
X=22.2g
Y=27g
Z=4.4g
Cu2 (OH) 2CO3%=
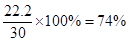 …………………………………………1分
…………………………………………1分C%=
 …………………………………………1分
…………………………………………1分
练习册系列答案
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案
相关题目