题目内容
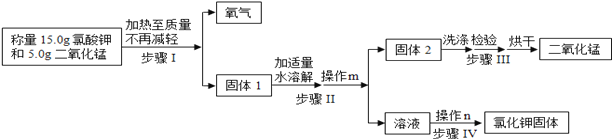
【题目】某污水中除含有少量泥沙外,还含有Ca2+、Mg2+、Na+、Cl-、SO![]() -等离子,为充分利用资源,科研小组设计了如下流程回收几种离子:
-等离子,为充分利用资源,科研小组设计了如下流程回收几种离子:
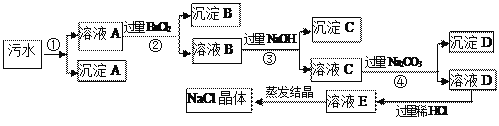
(1)①②③④步骤均有一个相同的操作步骤;此操作步骤必须用到的玻璃仪器有:烧杯、玻璃棒、__________;
(2)沉淀B的化学式为______________;
(3)加入过量稀盐酸可除去的物质有__________________________;
(4)步骤③中反应的方程式为_______________________________________________。
【答案】 漏斗 BaSO4 NaOH和Na2CO3 MgCl2+2NaOH=Mg(OH)2↓+2NaCl
【解析】(1)①②③④步骤中均有一个过滤操作,过滤操作必须用到的玻璃仪器有:烧杯、玻璃棒、漏斗;(2)在溶液A中加入过量的, ![]() 只有硫酸根离子会与钡离子产生沉淀,所以沉淀B是硫酸钡,化学方程式为:
只有硫酸根离子会与钡离子产生沉淀,所以沉淀B是硫酸钡,化学方程式为: ![]() ;(3)加入过量的稀盐酸可以除去第③步加入过量的氢氧化钠和第④步加入的过量的碳酸钠溶液;(4)溶液B中没有硫酸根离子,可能含有
;(3)加入过量的稀盐酸可以除去第③步加入过量的氢氧化钠和第④步加入的过量的碳酸钠溶液;(4)溶液B中没有硫酸根离子,可能含有![]() 、
、![]() 、
、![]() 、
、![]() 和
和![]() ,加入过量氢氧化钠溶液后,氢氧化钠会与镁离子、氯离子发生反应生成氢氧化镁沉淀和氯化钠,化学方程式为:
,加入过量氢氧化钠溶液后,氢氧化钠会与镁离子、氯离子发生反应生成氢氧化镁沉淀和氯化钠,化学方程式为: ![]() 。
。

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案【题目】某化学兴趣小组的同学对有关氧气方面进行探究
探究一:对空气中氧气含量的测定实验进行探究:
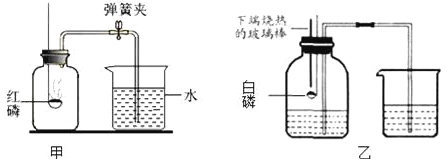
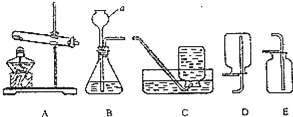
(1)如图甲所示装置和药品进行实验,集气瓶中发生反应的文字或符号表达式为__________。
(2)该组同学做了6次实验,整理数据如下:
1 | 2 | 3 | 4 | 5 | 6 | |
进入集气瓶中水的体积(mL) | 20 | 21 | 19 | 20 | 22 | 18 |
(注:集气瓶容积为100mL)通过6次实验,该组同学探究出氧气约占空气体积的_________。
(3)小林同学利用甲图装置测定空气中氧气的含量,下列操作会使测定结果偏小的是(_______)
A、实验装置可能漏气
B、实验中所取的红磷过量
C、实验前没有将弹簧夹夹紧
D、红磷燃烧结束后,没等装置冷却就打开弹簧夹
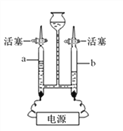
(4)小组内同学查阅资料后知道白磷40℃即燃烧,燃烧产物与红磷相同,于是采用改进后的乙装置进行重新探究.主要操作是:在实际容积为100mL的集气瓶里先装进30mL的水,再按图连好仪器,按下热的玻璃棒,白磷立即被点燃.
①白磷从燃烧到熄灭冷却的过程中,瓶内水面的变化是____________,若实验非常成功,最终集气瓶中水的体积约为______________mL.
②你认为集气瓶里预先装进的水有哪些作用?(____________)(填序号)
a.加快集气瓶冷却 b.液封导气管末端以防气体逸出 c.缓冲集气瓶内气压的骤然升高