题目内容
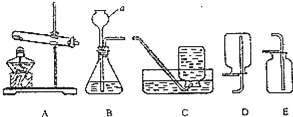
【题目】如图为实验室常用的制取和收集气体的装置,请回答下列问题.
(1)仪器a的名称是________.
(2)实验室选择装置A且用高锰酸钾制取氧气时:
①你认为A装置存在的问题是______;
②该反应的化学方程式是______;
③若选用C做收集装置时,实验结束,停止加热前一定要先将导管移出水面,目的是______.
(3)实验室可用选择装置______(填序号)制取并收集CO2气体,该反应的化学方程式是__________________.
【答案】 长颈漏斗 试管口无棉花 2KMnO4![]() K2MnO4+MnO2+O2↑ 防止水倒流入试管,把试管炸裂 BE CaCO3+2HCl=CaCl2+CO2↑+H2O
K2MnO4+MnO2+O2↑ 防止水倒流入试管,把试管炸裂 BE CaCO3+2HCl=CaCl2+CO2↑+H2O
【解析】(1)仪器a的名称是:长颈漏斗.(2)实验室选择装置A且用高锰酸钾制取氧气时:①A装置中试管口应放一团棉花防止高锰酸钾颗粒堵塞导管; ②高锰酸钾在加热条件下生成锰酸钾、二氧化锰、氧气,该反应的化学方程式是2KMnO4![]() K2MnO4+MnO2+O2↑;③若选用C做收集装置时,实验结束,停止加热前一定要先将导管移出水面,目的是防止水倒流入试管,把试管炸裂;(3)实验室常用石灰石和稀盐酸反应制取CO2气体,可用选择固液常温型发生装置B,碳酸钙和稀盐酸反应生成二氧化碳气体、水、氯化钙,该反应的化学方程式是CaCO3+2HCl=CaCl2+CO2↑+H2O。
K2MnO4+MnO2+O2↑;③若选用C做收集装置时,实验结束,停止加热前一定要先将导管移出水面,目的是防止水倒流入试管,把试管炸裂;(3)实验室常用石灰石和稀盐酸反应制取CO2气体,可用选择固液常温型发生装置B,碳酸钙和稀盐酸反应生成二氧化碳气体、水、氯化钙,该反应的化学方程式是CaCO3+2HCl=CaCl2+CO2↑+H2O。

【题目】维生素C是一种人体必需的维生素。查阅资料可知下列信息:
部分性质 | 生理作用 | |
维生素C 化学式:C6H806 | 无色晶体,易溶于水;在酸性溶液中稳定,中性或碱性溶液中易被空气氧化…… | 促进人体生长发育,增强人体对疾病的抵抗能力…… |
请参与下列问题的讨论。
(1)维生素C中碳、氢、氧三种元素的质量比为_________。现有黄瓜、馒头、牛肉,其中富含维生素C的是____________。
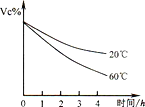
(2)某兴趣小组的同学对维生素C的还原性进行实验探究,其实验结果如图所示。实验说明了维生素C在空气中氧化除跟氧气有关外,还与_________有关。因此,生吃新鲜蔬菜要比熟吃蔬菜维生素C的损失__________ (选填“大”或“小”)。
(3) ①该兴趣小组同学对某果计饮料中维生素C的含量进行测定,反应原理为: C6H806+I2==C6H606 +2HI
实验步骤如下:
a.取果汁饮料10 mL,用煮沸并冷却的蒸馏水稀释到50 mL
b.加醋酸溶液酸化 c.加人少量指示剂
d.逐滴加人稀碘水至完全反应,实验测得恰好反应时,消耗溶质碘的质量为25.4mg。计算该果汁饮料每100mL中含维生素C的质量为______________mg?
②有些同学在测定时,未加人醋酸溶液酸化,测得维生素C的含量明显小于其他同学。其原因是
__________________________________
【题目】下列有关说法中正确的是( )
A. 氧气在低温、高压的条件下可以转变为液体或固体
B. 有颜色改变的变化一定是化学变化
C. 氧气的化学性质比较活泼,是可燃物
D. 通常情况下,空气的成分是比较固定的
【题目】Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件。某化学兴趣小组的同学为了测定某黄铜的组成,取40g该黄铜样品于烧杯中,向其中分5次加入相同溶质质量分数的稀硫酸,使之充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
加入稀硫酸的质量(g) | 充分反应后剩余固体的质量(g) | |
第1次 | 40 | 34.8 |
第2次 | 40 | 29.6 |
第3次 | 40 | 24.4 |
第4次 | 40 | 24.0 |
第5次 | 40 | m |
试回答下列问题:
(1)上述表格中m的值为多少?
(2)黄铜样品中锌的质量分数是多少?
(3)所用稀硫酸中硫酸的质量分数是多少?