题目内容
【题目】在“创新实验装置”的竞赛中,某化学兴趣小组设计了如图所示的装置(夹持仪器已略去),引起同学们的兴趣.如图是四位同学对实验中的部分现象进行的预测,预测正确的是
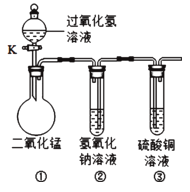
A. 打开活塞K,装置①中会有气泡冒出,黑色固体消失
B. 打开活塞K,装置②中会看到液面上升,产生蓝色沉淀
C. 打开活塞K,装置②中会有气泡冒出
D. 打开活塞K,装置③中会有液体流入,产生蓝色沉淀
【答案】D
【解析】A. 打开活塞K,装置①中过氧化氢溶液滴入烧瓶内,在二氧化锰的作用下分解生成水和氧气,会有气泡冒出;二氧化锰是过氧化氢分解的催化剂,反应前后质量和化学性质不变,黑色固体不会消失;B. 打开活塞K,装置①中生成的氧气进入装置②中,装置②中压强增大,在压力的作用下,试管内液面下降,导管内液面上升; C. 打开活塞K,装置①中生成的氧气进入装置②中,但由于气体在液面上,装置②中不会有气泡冒出;D. 打开活塞K,装置①中生成的氧气进入装置②中,装置②中压强增大,在压力的作用下,试管内液面下降,导管内液面上升,使装置②中的氢氧化钠溶液流入③中,氢氧化钠和硫酸铜反应产生蓝色氢氧化铜沉淀和硫酸钠。选D

【题目】分类、类比是同学们学习化学获取知识的重要科学方法。
(1)氧化反应在生活中随处可见,下面是常见的氧化反应:
|
|
|
|
A动植物呼吸 | B生活火灾 | C金属锈蚀 | D火药爆炸 |
请你将上述氧化反应平均分成两组,其中一组是__________;比较B和D,图D发生的现象除了具备B中条件外,还必须具备的另一个条件是________________。
(2)在元素周期表中,C与Si所处的位置及结构如图

已知二氧化碳与氢氧化钠溶液反应如下
CO2+2NaOH=Na2CO3+H2O
装有氢氧化钠溶液的细口瓶,瓶口磨砂后暴露出SiO2,请你写出二氧化硅与氢氧化钠溶液的反应方程式为_________________,生成物是玻璃胶的成分,因此装有氢氧化钠溶液的细口瓶应用__________塞。