题目内容
【题目】下列有关计算及结果,不正确的是
A. 氢氧化镁(Mg(OH)2)的相对分子质量=24 +(16+1)×2 = 58
B. 硫酸铜[CuSO4]中各元素的质量比为铜∶硫∶氧 = 2∶1∶2
C. 尿素(CO(NH2)2)中各元素的原子数目比为碳:氧:氮:氢=1∶1∶1∶4
D. 氢氧化钠(NaOH)中氧元素的质量分数=![]()
【答案】C
【解析】
A、氢氧化镁【Mg(OH)2】的相对分子质量=24 +(16+1)×2 = 58,选项正确;B、硫酸铜[CuSO4]中各元素的质量比为铜∶硫∶氧=64:32:16×4=2∶1∶2,选项正确;C、尿素【CO(NH2)2】中各元素的原子数目比为碳:氧:氮:氢=1:1:1×2:1×4=1:1:2:4,选项错误;D、氢氧化钠【NaOH】中氧元素的质量分数=![]() ,选项正确。故本题选C。
,选项正确。故本题选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】质量守恒定律对科学发展具有重大意义。
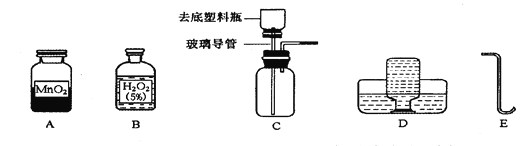
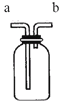
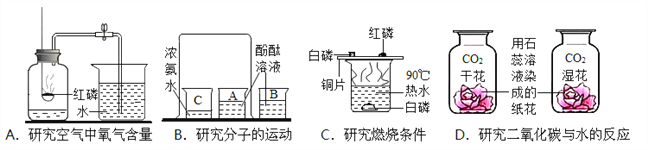
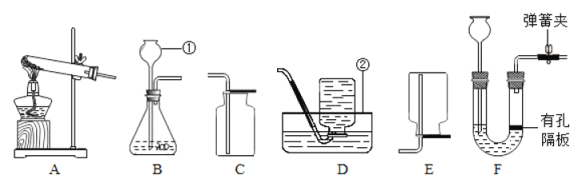
Ⅰ.用如图所示的 3 个实验装置进行验证质量守恒定律的实验,其中不能达到实验目的是_____(填序号),其原因是_____。

Ⅱ.A 图是测定红磷燃烧前后质量的变化情况,用来验证质量守恒的实验,试回答:
(1)红磷燃烧的化学方程式是_____。
(2)在这个实验中气球的作用是_____。
(3)将橡皮塞上的玻璃管放在酒精灯上灼烧到红热后,迅速用橡皮塞将锥形瓶塞紧,并将红磷引燃,这里要“迅速用橡皮塞将锥形瓶塞紧”的原因是_____。
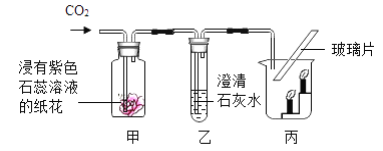
Ⅲ.C 中反应的化学方程式是_____。
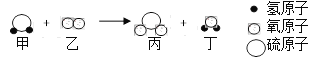
Ⅳ.在不同时刻,某反应中的甲、乙、丙、丁四种物质的质量如下表。已知甲的相对分子质量为丁的 2 倍,则下列说法不正确的_____。
甲的质量/g | 乙的质量/g | 丙的质量/g | 丁的质量/g | |
反应前 | 64 | 10 | 1 | 16 |
t 时刻 | 32 | a | ||
反应后 | 0 | 42 | b | 48 |
A.该反应的基本类型是分解反应 B.a 等于 32
C.丙可能是催化剂 D.该反应方程式中甲与丁的化学计量数之比为 2:1