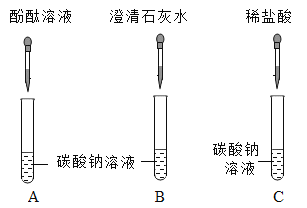
题目内容
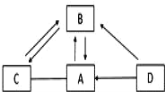
【题目】超细碳酸钙可用于生产钙片、牙膏等产品。利用碳化法生产超细碳酸钙的主要流程示意图如下:
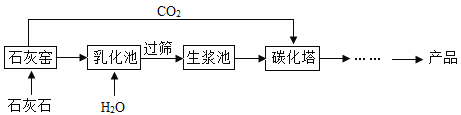
(1)乳化池中,生石灰与水发生反应,其化学方程式为_________
(2)乳化池中的物质通过“过筛”可以拦截大于筛孔直径的颗粒,相当于基本实验操作中的_____。
(3)碳化塔中反应的化学方程式为____________。
【答案】![]() 过滤
过滤 ![]()
【解析】
(1)乳化池中,生石灰与水发生反应生成氢氧化钙,其化学方程式为:CaO+H2O=Ca(OH)2;
(2)乳化池中的物质通过“过筛”可以拦截大于筛孔直径的颗粒,相当于基本实验操作中的:过滤。
(3)向碳化塔中的氢氧化钙溶液中通入二氧化碳气体反应生成碳酸钙沉淀和水,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】探究影响化学反应速率的因素。
(1)[发现和提出问题]
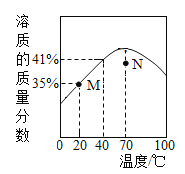
镁在空气中能够剧烈燃烧,铁丝在氧气中能够剧烈燃烧,而真金不怕火炼,这说明决定物质之间能否发生反应以及反应速率的内因是______。蜡烛在氧气中燃烧比在空气中燃烧剧烈,这一事例中影响化学反应速率的因素是______;夏天,将食品放在冰箱里不容易变质,这一事例说明温度也能影响化学反应速率。温度如何影响反应速率呢?
(2)[猜想与假设]
温度越高,反应速率越快。
(3)[收集证据]
实验药品:颗粒大小相同的锌粒:两份相同溶质质量分数、不同温度的稀硫酸(20℃、40℃)。
供选仪器:药匙、气体发生装置2套(气密性良好)、量筒2支、分液漏斗、秒表、胶头滴管、水槽、大试管2支。
利用上述仪器和药品,补充完成下表的实验报告。
观察或测量的量 | 实验步骤 | 实验现象 | 实验结论 |
产生相同体积(一试管)的气体所需要的时间 | ①分别取相同数量(或质量)锌粒于两套气体发生装置中 ②______ ③记录收集一试管气体所需的时间 | ④______ | 温度越高、反应速率越快 反应的化学方程式是 ⑤______ |
(4)[结论与解释]
从微观的角度分析“温度越高,反应速率越快"的原因是___________。
(5)[拓展分析]
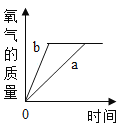
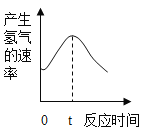
根据其他测定方法,实验小组的同学绘制了锌粒与稀硫酸反应产生氢气的速率随时间变化的曲线,如图所示。请据图分析:时间0-t内,反应速率逐渐加快的主要原因是________,时间t以后,反应速率逐渐减慢的主要原因是________________。
【题目】请结合下图回答下列问题。
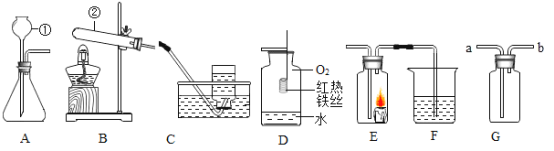
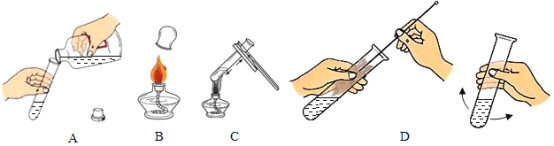
(1)请写出图中标号仪器的名称:①_________;②_________.
(2)选择B装置制氧气的文字表达式为_________, 选择C装置收集氧气的原理是_________, D中水的作用是_________。
(3)某同学连接A、E、F进行实验,若实验时E中蜡烛燃烧更旺,F 中澄清石灰水变浑浊,则仪器①中所加药品为_________, A中发生反应的文字表达式_________, F中澄清石灰水变浑浊的原因是_________。
(4)实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下氨气是一种无色有刺激性气味的气体,密度比空气小,极易溶于水。制取并收集氨气,应从上图中选择_________。
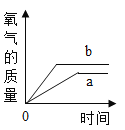
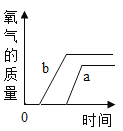
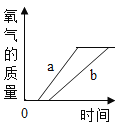
(5)实验室加热一定量高锰酸钾固体制取氧气时,如图所示,表示某物质随时间变化的关系,则纵坐标表示的是_________。

a.高锰酸钾的质量 b.氧气的质量 c.二氧化锰的质量 d.试管中剩余固体物质质量
(6)带火星木条在氧气中可以复燃。那么,是不是只有纯净的氧气才能使带火星的木条复燃呢?为此,同学们开展了相关的实验探究。实验主要步骤如下:先制取一定量的氧气备用,再测得集气瓶实际容积为317 mL,然后采用某种正确的收集方法得到5瓶氧气含量不同的气体,最后用带火星的木条来检验,观察木条是否复燃,相关的数据见下表:
集气 编号 | 瓶内预装水体积/mL | 充入氧气体积/ mL | 瓶内空气体积/mL | 瓶内空气里氧气的体积分数 | 木条能不能复燃 |
1 | 120 | 120 | 197 | 50.9% | 能 |
2 | 97 | 97 | 220 | 能 | |
3 | 90 | 90 | 227 | 43.4% | 能 |
4 | 84 | 84 | 233 | 41.9% | 能 |
5 | 81 | 81 | 236 | 41.2% | 不能 |
表中空格处应填______,由该实验可得到的结论是_______。