题目内容
实验室常用一定质量分数的过氧化氢溶液制取氧气.某同学取2g二氧化锰于锥形瓶中,然后慢慢滴入34g过氧化氢溶液,完全反应后,称得锥形瓶内剩余物质的总质量是34.4g.
求:(1)生成氧气的质量.
(2)该同学所用过氧化氢溶液中溶质质量分数.
解:根据质量守恒定律可知氧气的质量是:34g+2g-34.4g=1.6g
设要生成1.6g氧气需要参加反应的过氧化氢的质量为X,则:
2H2O2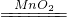 2H2O+O2↑
2H2O+O2↑
68 32
x 1.6g
根据: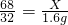 解得X=3.4g,所以所用过氧化氢溶液中溶质质量分数为:
解得X=3.4g,所以所用过氧化氢溶液中溶质质量分数为: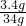 ×100%=10%..
×100%=10%..
故答案为:
(1)1.6g;
(2)10%.
分析:根据锥形瓶内质量的减少量就是生成的氧气的质量,根据氧气的质量算出过氧化氢的质量,再除以过氧化氢溶液的质量乘以百分之百即可.
点评:解答本题的关键是根据质量守恒定律可知锥形瓶内质量的减少量就是生成氧气的质量.再根据方程式进行进一步的计算即可.
设要生成1.6g氧气需要参加反应的过氧化氢的质量为X,则:
2H2O2
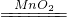 2H2O+O2↑
2H2O+O2↑68 32
x 1.6g
根据:
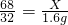 解得X=3.4g,所以所用过氧化氢溶液中溶质质量分数为:
解得X=3.4g,所以所用过氧化氢溶液中溶质质量分数为: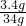 ×100%=10%..
×100%=10%..故答案为:
(1)1.6g;
(2)10%.
分析:根据锥形瓶内质量的减少量就是生成的氧气的质量,根据氧气的质量算出过氧化氢的质量,再除以过氧化氢溶液的质量乘以百分之百即可.
点评:解答本题的关键是根据质量守恒定律可知锥形瓶内质量的减少量就是生成氧气的质量.再根据方程式进行进一步的计算即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
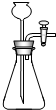 检验时所发生反应的化学方程式.
检验时所发生反应的化学方程式.
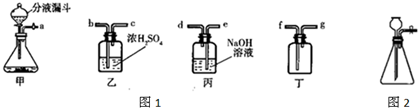
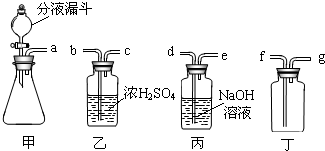
 实验室常用亚硝酸钠(NaNO2)与氯化铵溶液(NH4Cl)反应制取N2.N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3.下图为制取少量NH3并检验NH3的装置(制取H2的装置已略去):
实验室常用亚硝酸钠(NaNO2)与氯化铵溶液(NH4Cl)反应制取N2.N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3.下图为制取少量NH3并检验NH3的装置(制取H2的装置已略去):