题目内容
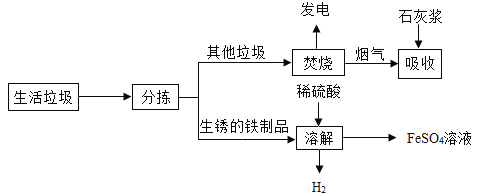
【题目】城市生活垃圾的处理是世界性难题。某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如下:
资料1:垃圾焚烧产生的烟气中含有SO2,HCl等有害气体;
资料2:+2价的铁元素容易被空气中的氧气氧化。
回答下列问题:
(1)焚烧垃圾发电厂是将垃圾焚烧后获得的_____能最终转化为电能。
(2)在上述流程的“吸收”步骤中,石灰浆的作用是_____。
(3)在上述流程的“溶解”步骤中,发生反应的化学方程式除![]() 外还有2个反应,其中有单质生成的化学方程式是_____。
外还有2个反应,其中有单质生成的化学方程式是_____。
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、过滤,得到硫酸亚铁晶体,其中氮气的作用是_____。
(5)将无水硫酸亚铁(FeSO4)隔绝空气加强热,产物有氧化铁和其它两种硫的氧化物,试写出该反应的化学方程式_____。
【答案】热 除去烟气中含有的SO2、HCl ![]() 作保护气,防止+2价的铁元素被空气中的氧气氧化
作保护气,防止+2价的铁元素被空气中的氧气氧化 ![]()
【解析】
(1)发电厂利用垃圾焚烧,焚烧的过程中放出大量的热,从而将产生的热能转变为电能。故答案为:热;
(2)石灰浆是氢氧化钙溶液,溶液显碱性,能够吸收酸性气体。该步骤中会产生二氧化硫、氯化氢等酸性气体。所以吸收步骤中,石灰浆的作用是除去烟气中含有的SO2、HCl。故答案为:除去烟气中含有的SO2、HCl;
(3)溶解步骤中,共计发生三个反应。铁锈和硫酸反应生成硫酸铁和水。待铁锈被腐蚀后,内部的金属铁和硫酸反应生成硫酸亚铁和氢气。同时在发生硫酸铁和铁单质反应生成硫酸亚铁。除题干之外的两个反应中,铁和硫酸反应生成硫酸亚铁和氢气,氢气属于单质。所以产生的H2的化学方程式为![]() 。故答案为:
。故答案为:![]() ;
;
(4)硫酸亚铁在空气中,容易被空气中的氧气氧化,从而转化为硫酸铁。而氮气的化学性质稳定,其中氮气的作用是作保护气,避免+2价的铁元素被空气中的氧气氧化。故答案为:作保护气,防止+2价的铁元素被空气中的氧气氧化;
(5)硫酸亚铁在加热的条件下生成氧化铁和另外的硫的两种氧化物。硫常见的氧化物二氧化硫和三氧化硫。故答案为:![]() 。
。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案【题目】化学实验是我们应用化学知识、拓展化学思维和培养化学素养的重要途经。如下图所示,在一只烧杯中进行实验,认真分析实验步骤,不能达到预期效果或目的的是( )
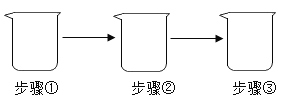
序号 | 目的 | 步骤 |
A | 探究盐酸能否与氢氧化钠发生反应 | ①加入NaOH溶液;②滴加酚酞溶液; ③加入适量盐酸 |
B | 检验NaCl中混有Na2CO3 | ①加入少量样品;②加入适量水至全部溶解;③加入适量氢氧化钙溶液 |
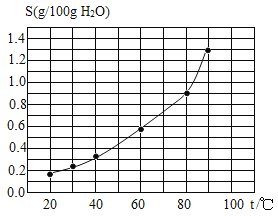
C | 验证KCl不能无限溶解 | 20℃时:①加入100g水;②加入15gKCl;③加入15gKCl。(已知:20℃时,KCl的溶解度为34g) |
D | 配制50g溶质质量分数为5%的氯化钠溶液 | ①加入2.5gNaCl;②加入47.5g水;③搅拌至全部溶解 |
A.AB.BC.CD.D