题目内容
【题目】请你应用质量守恒定律完成下列各题。
(1)世博会已有千辆新能源汽车投入运行,其中部分公交车采用二甲醚(C2H6O)做燃料。二甲醚分子中C、H、O元素的原子个数比为 。
(2)某化合物在纯氧中充分燃烧后,只生成水和二氧化碳,该物质中 。
A. 只含有碳元素
B. 只有氢元素
C. 一定含有碳、氢两种元素,可能含有氧元素
D. 一定有碳、氢、氧三种元素
(3)黑火药点燃时发生如下反应:2KNO3+S+3C![]() K2S+3CO2↑+X↑,其中X的化学式为 。
K2S+3CO2↑+X↑,其中X的化学式为 。
(4)下图给出的是某反应在同一容器中反应前后的分子种类。
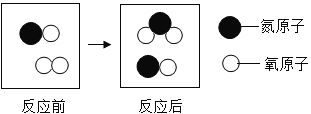
反应前 反应后
①化学反应中,参加反应的![]() 和生成的
和生成的![]() 的质量比为 。
的质量比为 。
②由此可知,在化学反应前后,一定不变的是 (填数字序号)。
a. 原子种类 b. 原子数目 c. 分子种类
d. 分子数目 e. 元素种类 f. 物质的总质量
【答案】(1)2:6:1 (2)C (3)N2
(4)8:23 abef(共2分,少选一个给1分)
【解析】
(1)利用化学式的含义进行解答;
(2)根据质量守恒定律可知,化学反应前后元素的种类不变,进行判断;
(3)根据质量守恒定律可知,化学反应前后原子的种类和个数不变,进行判断;
(4)①由分子构成确定物质的化学式,写出反应的化学方程式,计算反应中指定物质的质量比;②以不变应万变,在化学反应中记住这些肯定不变的吧:物质的总质量、元素的种类、元素的质量、原子的种类、原子的质量、原子的数目.
解答:解:(1)由二甲醚的化学式C2H6O可知,C、H、O元素的原子个数比为2:6:1;
(2)因为生成物二氧化碳和水中含有C、H、O三种元素,所以反应物中也应该有这三种元素,又知某物质在氧气中充分燃烧,故生成物中的氧元素可能来自氧气,故可判断该物质中一定含有碳、氢元素,可能含有氧元素;
(3)根据质量守恒定律可知,化学反应前后原子的种类和个数不变,一起来数一数原子的数目,看一看元素的种类,你会判断出X的化学式为N2;
(4)①图示为NO和O2反应生成NO2,该反应的化学方程式为2NO+O2═2NO2;反应中O2与NO2的质量比=32:(2×46)=8:23;②根据质量守恒定律可知,在化学反应中记住这些肯定不变的吧:物质的总质量、元素的种类、元素的质量、原子的种类、原子的质量、原子的数目,故一定不变的是一定不变的是.
故答案为(1)2:6:1;(2)C;(3)N2;(4)①8:23;②abef.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】小苏打(碳酸氢钠)在日常生活中有广泛的用途,工业上制取小苏打有多种方法,其中有一种是气相固碳法,其利用的原理是: ![]()
[资料]碳酸钠和碳酸氢钠的溶解度表(一个标准大气压下) (部分)
温度/°C | 0 | 15 | 20 | 30 | 40 | 50 | 60 |
碳酸氢钠溶解度/g | 6.9 | 8.72 | 9.6 | 11.1 | 12.7 | 14.45 | 16.4 |
碳酸钠溶解度/g | 7.1 | 13.25 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 |
学校实验小组验证反应原理,在室温为15℃时,同学们将10g氢氧化钠固体完全溶于80g水中,而后匀速的通人二氧化碳气体,同时用传感器测定溶液的pH变化如图一所示,并同时用数据采集器记录并绘制图像如图2所示。

[分析与判断]
(1) 通过图象分析,小苏打溶液是显________(填“酸性”、“中性”或“碱性”),图像中M点处发生的主要化学反应方程式为________________________。
(2)为了确定M处溶液的成分,同学们进行了如下的探究:
[提出猜想]
猜想一:可能是Na2CO3
猜想二:可能是Na2CO3、NaOH
[实验探究]
实验步骤 | 加入试剂 | 实验现象 | 初步实验结论 |
① | 滴人酚酞溶液 | _________ | 猜想二正确 |
② | 加入_________溶液 | _________ |
[实验反思]实验过程中,同学们发现18min 后溶液的pH基本不再变化,则此时烧杯中可观察到的现象有_____________________。
【题目】某兴趣小组对石灰石样品进行如下实验分析,取48.0g样品放入质量为100.0g的烧杯中,将150.0g稀盐酸分3次加入烧杯中,充分反应后(杂质不溶于水,也不与酸反应),测得烧杯及其内物质的质量记录如下。
次数 | 1 | 2 | 3 |
加入稀盐酸的质量/g | 50.0 | 50.0 | 50.0 |
烧杯及其内物质的质量/g | 190 | 232 | 278 |
请计算:
(1)样品中CO2的质量为_________________g。
(2)所用稀盐酸的溶质的质量分数___________