题目内容
【题目】用图1和图2两个实验装置探究分子的性质。

(1)图1实验观察到的现象是_____,由此得出的结论是_____。
(2)图2中电子天平示数变小,从微粒的角度解释其原因是_____。
【答案】C管中的溶液比B管中的溶液先由无色变红,A和D无明显现象 温度越高,氨分子运动速率越快 水分子从量筒中运动到空气中
【解析】
(1)图1实验观察到的现象是C管中的溶液比B管中的溶液先由无色变红,A和D无明显现象,由此得出的结论是温度越高,氨分子运动速率越快。
故填:C管中的溶液比B管中的溶液先由无色变红,A和D无明显现象;温度越高,氨分子运动速率越快。
(2)水在空气中蒸发质量减少,图2中电子天平示数变小,从微粒的角度解释其原因是水分子从量筒中运动到空气中。
故填:水分子从量筒中运动到空气中。

 阅读快车系列答案
阅读快车系列答案【题目】今年扬州迎来高铁交通发展的高潮。高铁给我们带来的不仅是交通方便,出行快捷,甚至是带来旅游业的繁荣。制造铁轨需要大量的合金钢,新集中学化学兴趣小组为此展开探究:
(一)工业上炼铁炼钢和轧制钢材的主要流程如下图:
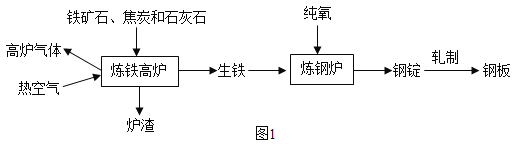
已知:生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%。
(1)炼铁的固体原料中加入焦炭的作用是_____,_____(用方程式表示);
(2)炼铁的固体原料需经过粉碎,其目的是_____;
(3)热空气和高炉气体的主要成分有一种相同,这种气体是_____(填化学式);
(4)炼钢炉中,通入纯氧而不用空气的目的是_____。将钢锭轧成钢板,体现了金属的_____性。
(二)该兴趣小组发现未经处理的钢铁容易生锈。同学们接着探究了铁生锈的相关问题。
(知识回顾)铁生锈的条件为铁与_____、_____同时接触,为了防止铁制品生锈,应采取的措施是_____(写出一种)。
(查阅资料)铁锈成分复杂,化学式可简单表示为Fe2O3nH2O,在加热时会分步反应,首先失去结晶水,其反应可表示为Fe2O3nH2O![]() Fe2O3+nH2O。浓硫酸可以吸水,碱石灰可以吸收水和二氧化碳。
Fe2O3+nH2O。浓硫酸可以吸水,碱石灰可以吸收水和二氧化碳。
(提出问题)铁锈(Fe2O3nH2O)中n的值等于多少呢?
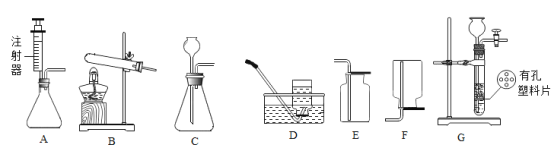
(问题探究)小明发现实验室中有一保管不善的铁粉,大部分已经结块成红褐色,为了探究铁锈(Fe2O3nH2O)的组成,称取27.0g这种铁粉样品,按如图2所示装置进行实验。
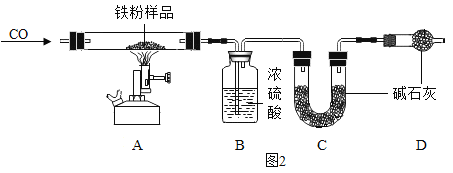
(1)实验前应先_____;
(2)为了保证实验安全,实验开始时应先_____,目的是_____;
(3)D的作用是_____;
(4)请指出该装置中有一处明显不足_____;
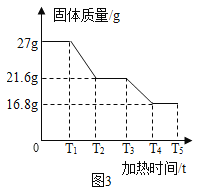
(数据处理)图3是加热时间和A中固体质量关系图象,下表是B、C中质量不再变化时B中浓硫酸、C中碱石灰装置质量变化情况。
反应前(g) | 反应后(g) | |
B | 100 | 105.4 |
C | 150 | 163.2 |
(5)铁锈(Fe2O3nH2O)中n的值是_____;
(6)写出T3﹣T4时间段发生反应的化学方程式_____;
(7)计算原样品中单质铁的质量分数是_____。(计算结果保留到0.1%)