题目内容
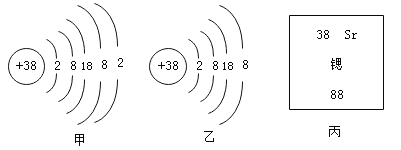
【题目】如图所示是5种粒子结构示意图,回答下列问题:
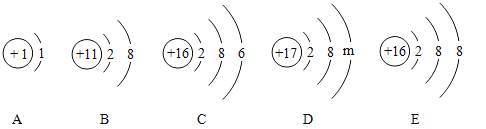
(1)示意图中的元素,它们之间本质区别是_________不同;属于同种元素的是_________。
(2)A、B、C、E中属于阴离子的是_________。(填离子符号)
(3)若D表示某元素的原子,则m=__________,该粒子在化学变化中容易____(填“得”或“失”)电子形成化合物,此时该元素的化合价为_________。
(4)写出B与E组成的化合物的化学式_______。
【答案】质子数(或核电荷数) CE E 7 得 -1 Na2S
【解析】
(1)质子数(或核电荷数)决定元素的种类,故属于同种元素的是CE;
(2)核内质子数<核外电子数的属于阴离子,故A、B、C、E中属于阴离子的是E;
(3)若D表示某元素的原子,由于在原子中核内质子数=核外电子数,则m=17-2-8=7,最外层电子数大于4,该粒子在化学变化中容易得到1个电子形成稳定结构,此时该元素的化合价为-1;
(4)根据结构示意图可知,B是Na+,E是S2-,B与E组成的化合物的化学式为Na2S。

练习册系列答案
 启东小题作业本系列答案
启东小题作业本系列答案
相关题目